摘要:研究人员已经确定了导致阿尔茨海默病患者线粒体功能障碍的机制。
美因茨约翰内斯·古腾堡大学(JGU)的一组研究人员已经确定了导致阿尔茨海默病患者线粒体功能障碍的机制,从而导致大脑能量供应减少。JGU制药和生物医学科学研究所的克里斯蒂娜·弗里德兰教授说:“这种效应可归因于一种以前未被报道过的RNA修饰。”她与同事Mark Helm教授合作指导了相关研究。他们的研究结果有助于更好地理解阿尔茨海默病的病理生理学。美因茨大学医学中心、分子生物学研究所、洛林大学和维也纳医科大学的研究小组也参与了这项研究。相应的论文发表在《分子精神病学》上。

图1 ND5 mRNA中腺苷(m1A)的N1甲基化导致阿尔茨海默病的复合物I功能障碍
受功能紊乱影响的“细胞发电站”
线粒体通常被称为细胞的动力源,是细胞内的细胞器,负责向全身尤其是大脑提供能量。大脑95%的能量依赖于线粒体中的葡萄糖代谢。人们早就知道,葡萄糖代谢障碍发生在阿尔茨海默病的早期阶段。这种损伤是由于衰老过程和β淀粉样蛋白的积累引起的线粒体功能失调。
三磷酸腺苷(ATP)形式的能量来源通过呼吸链的一系列反应在线粒体内膜形成。参与这一过程的有一千多种蛋白质,它们从细胞核运输到线粒体。“但也有一些蛋白质是由线粒体自己合成的。其中之一是ND5,它是呼吸链复合体I的一个亚基,”克里斯蒂娜·弗里德兰教授解释说。一种叫做NADH的物质给复合体I提供电子,复合体I将电子转移给泛醌,产生泛醇。在这个过程中,四种蛋白质从基质中被泵入膜间空间。ND5在这一联系中起着重要作用,该亚基的线粒体编码基因的任何突变都可能导致严重的线粒体疾病,如Leigh综合征。
已经证明,为这种蛋白质的合成提供指令的mRNA可以经历甲基化。在体细胞中,mRNA携带遗传信息,并与tRNA一起负责将遗传信息翻译成蛋白质。mRNA的甲基化导致其化学结构的改变,使其不能再正确地与tRNA相互作用。弗里德兰补充说:“合成过程被破坏,形成的ND5亚基蛋白质更少,而ND5是复合物I的核心相关蛋白,因为整个过程始于呼吸链。”
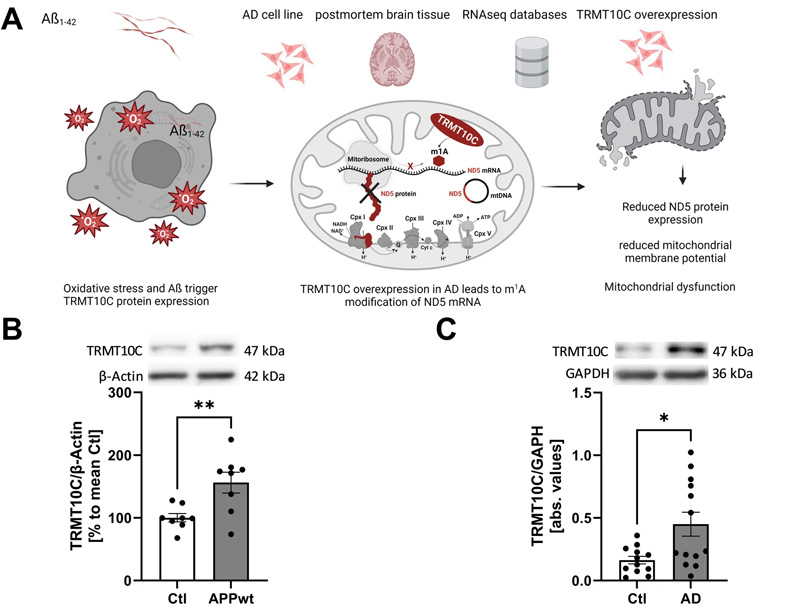
图2 TRMT10C蛋白和mRNA水平在AD细胞和动物模型以及AD患者的皮层样本中增加
TRMT10C酶引起甲基化,从而抑制ND5的合成
美因茨大学制药和生物医学科学研究所的弗里德兰和赫尔姆团队能够证明,是一种名为TRMT10C的酶诱导了这种甲基化,从而随后抑制了ND5。研究人员在合适的细胞模型和阿尔茨海默病患者的大脑中观察到ND5亚基蛋白质的生物合成受到抑制。
正如作者在《分子精神病学》上发表的文章中所述:“因此,我们首次证明,TRMT10C诱导ND5 mRNA的m1A甲基化导致线粒体功能障碍。我们的研究结果表明,这种新发现的机制可能与a β诱导的线粒体功能障碍有关。”该研究由Transregio 319合作研究中心“RMaP: RNA修饰和加工”的一部分资助。
参考资料
[1] N1-methylation of adenosine (m1A) in ND5 mRNA leads to complex I dysfunction in Alzheimer’s disease
摘要:研究人员已经确定了导致阿尔茨海默病患者线粒体功能障碍的机制。
美因茨约翰内斯·古腾堡大学(JGU)的一组研究人员已经确定了导致阿尔茨海默病患者线粒体功能障碍的机制,从而导致大脑能量供应减少。JGU制药和生物医学科学研究所的克里斯蒂娜·弗里德兰教授说:“这种效应可归因于一种以前未被报道过的RNA修饰。”她与同事Mark Helm教授合作指导了相关研究。他们的研究结果有助于更好地理解阿尔茨海默病的病理生理学。美因茨大学医学中心、分子生物学研究所、洛林大学和维也纳医科大学的研究小组也参与了这项研究。相应的论文发表在《分子精神病学》上。

图1 ND5 mRNA中腺苷(m1A)的N1甲基化导致阿尔茨海默病的复合物I功能障碍
受功能紊乱影响的“细胞发电站”
线粒体通常被称为细胞的动力源,是细胞内的细胞器,负责向全身尤其是大脑提供能量。大脑95%的能量依赖于线粒体中的葡萄糖代谢。人们早就知道,葡萄糖代谢障碍发生在阿尔茨海默病的早期阶段。这种损伤是由于衰老过程和β淀粉样蛋白的积累引起的线粒体功能失调。
三磷酸腺苷(ATP)形式的能量来源通过呼吸链的一系列反应在线粒体内膜形成。参与这一过程的有一千多种蛋白质,它们从细胞核运输到线粒体。“但也有一些蛋白质是由线粒体自己合成的。其中之一是ND5,它是呼吸链复合体I的一个亚基,”克里斯蒂娜·弗里德兰教授解释说。一种叫做NADH的物质给复合体I提供电子,复合体I将电子转移给泛醌,产生泛醇。在这个过程中,四种蛋白质从基质中被泵入膜间空间。ND5在这一联系中起着重要作用,该亚基的线粒体编码基因的任何突变都可能导致严重的线粒体疾病,如Leigh综合征。
已经证明,为这种蛋白质的合成提供指令的mRNA可以经历甲基化。在体细胞中,mRNA携带遗传信息,并与tRNA一起负责将遗传信息翻译成蛋白质。mRNA的甲基化导致其化学结构的改变,使其不能再正确地与tRNA相互作用。弗里德兰补充说:“合成过程被破坏,形成的ND5亚基蛋白质更少,而ND5是复合物I的核心相关蛋白,因为整个过程始于呼吸链。”

图2 TRMT10C蛋白和mRNA水平在AD细胞和动物模型以及AD患者的皮层样本中增加
TRMT10C酶引起甲基化,从而抑制ND5的合成
美因茨大学制药和生物医学科学研究所的弗里德兰和赫尔姆团队能够证明,是一种名为TRMT10C的酶诱导了这种甲基化,从而随后抑制了ND5。研究人员在合适的细胞模型和阿尔茨海默病患者的大脑中观察到ND5亚基蛋白质的生物合成受到抑制。
正如作者在《分子精神病学》上发表的文章中所述:“因此,我们首次证明,TRMT10C诱导ND5 mRNA的m1A甲基化导致线粒体功能障碍。我们的研究结果表明,这种新发现的机制可能与a β诱导的线粒体功能障碍有关。”该研究由Transregio 319合作研究中心“RMaP: RNA修饰和加工”的一部分资助。
参考资料
[1] N1-methylation of adenosine (m1A) in ND5 mRNA leads to complex I dysfunction in Alzheimer’s disease



