摘要:一种新的CRISPR基因编辑工具,AsCas12f,比常用的Cas9小,已经被设计用于治疗遗传疾病的更高效率和效果。该工具在小鼠身上测试成功,可能会在人类身上应用更紧凑、更有效的基因组编辑技术。
到目前为止,你可能听说过CRISPR,这是一种基因编辑工具,它使研究人员能够替换和改变DNA片段。就像基因裁缝一样,科学家们一直在尝试“剪掉”使蚊子成为疟疾携带者的基因,改变粮食作物,使其更有营养、更美味,近年来还开始进行人体试验,以克服一些最具挑战性的疾病和遗传疾病。
CRISPR改善我们生活的潜力是如此惊人,以至于在2020年,研究人员詹妮弗·杜德纳(Jennifer Doudna)和艾曼纽尔·查彭蒂耶(Emmanuelle Charpentier)获得了诺贝尔化学奖,他们开发了最精确的CRISPR-Cas9工具。

图1 基于AsCas12f的紧凑型基因组编辑工具
但即使是Cas9也有局限性。将遗传物质传递到宿主细胞的常用方法是使用修饰过的病毒作为载体。腺相关病毒(AAV)对患者无害,可以进入许多不同类型的细胞,引入Cas9等CRISPR酶,与其他一些方法相比,引发不良免疫反应的可能性较低。然而,像任何包裹递送服务一样,有尺寸限制。
东京大学生物科学系的Osamu Nureki教授解释说:“Cas9处于这种大小限制的极限,因此需要一种更小的Cas蛋白,可以有效地包装成AAV并作为基因组编辑工具。”
它的大尺寸意味着Cas9在用于基因治疗时可能缺乏效率。因此,一个大型的多机构团队致力于开发一种更小的Cas酶,它同样活跃,但效率更高。研究人员选择了一种名为AsCas12f的酶,这种酶来自于硫氧化轴二芽孢杆菌。这种酶的优点是它是迄今为止发现的最紧凑的Cas酶之一,其大小不到Cas9的三分之一。
新设计的CRISPR酶提供了一种更紧凑的DNA编辑解决方案,保持了现有工具的效率,并可以改善患者的治疗。新的基于CRISPR的基因编辑工具可能会为患有遗传性疾病的患者带来更好的治疗方法。这种工具是一种名为AsCas12f的酶,它经过了修饰,可以提供同样的效果,但大小只有通常用于基因编辑的Cas9酶的三分之一。紧凑的尺寸意味着更多的它可以被装入载体病毒并传递到活细胞中,使其更有效。
在之前的测试中,AsCas12f在人类细胞中几乎没有任何基因组活性。
研究人员创建了一个可能的AsCas12f突变库,然后将选择的突变组合在一起,设计出一种编辑能力比原始未突变型高10倍的AsCas12f酶。这种基因工程的AsCas12f已经在小鼠身上成功进行了测试,并有可能在未来用于新的、更有效的治疗方法。
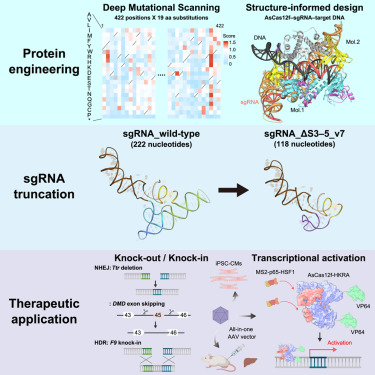
图2 AsCas12f编辑工具的应用
“使用一种称为深度突变扫描的筛选方法,我们通过用所有生命所基于的所有20种氨基酸取代AsCas12f的每个氨基酸残基,组装了一个潜在的新候选者库。由此,我们确定了200多个增强基因组编辑活性的突变,”Nureki解释说。“基于从AsCas12f的结构分析中获得的见解,我们选择并结合这些增强活性的氨基酸突变来创建一个修饰的AsCas12f。与通常的AsCas12f类型相比,这种工程AsCas12f具有10倍以上的基因组编辑活性,并且与Cas9相当,同时保持更小的尺寸。”
该团队已经对AsCas12f系统进行了动物试验,将其与其他基因结合起来,并将其施用于活小鼠。直接对人体进行治疗比提取细胞、在实验室对其进行编辑、再将其植入患者体内更可取,后者更耗时、更昂贵。测试的成功表明,经过改造的AsCas12f具有用于人类基因治疗的潜力,例如治疗血友病(一种血液不能正常凝结的疾病)。
该团队发现了许多潜在的有效组合,用于设计改进的AsCas12f基因编辑系统,因此研究人员承认,选择的突变可能不是所有可用组合中最理想的。下一步,计算建模或机器学习可以用来筛选组合,并预测哪些可能会提供更好的改进。
“提升AsCas12f以展示与Cas9相当的基因组编辑活性是一项重大成就,并且是开发新的,更紧凑的基因组编辑工具的重要一步,”Nureki说。“对我们来说,基因疗法的关键在于它真正帮助病人的潜力。使用我们开发的工程AsCas12f,我们的下一个挑战是实际实施基因治疗,以帮助患有遗传疾病的人。”
参考资料
[1] An AsCas12f-based compact genome-editing tool derived by deep mutational scanning and structural analysis
摘要:一种新的CRISPR基因编辑工具,AsCas12f,比常用的Cas9小,已经被设计用于治疗遗传疾病的更高效率和效果。该工具在小鼠身上测试成功,可能会在人类身上应用更紧凑、更有效的基因组编辑技术。
到目前为止,你可能听说过CRISPR,这是一种基因编辑工具,它使研究人员能够替换和改变DNA片段。就像基因裁缝一样,科学家们一直在尝试“剪掉”使蚊子成为疟疾携带者的基因,改变粮食作物,使其更有营养、更美味,近年来还开始进行人体试验,以克服一些最具挑战性的疾病和遗传疾病。
CRISPR改善我们生活的潜力是如此惊人,以至于在2020年,研究人员詹妮弗·杜德纳(Jennifer Doudna)和艾曼纽尔·查彭蒂耶(Emmanuelle Charpentier)获得了诺贝尔化学奖,他们开发了最精确的CRISPR-Cas9工具。

图1 基于AsCas12f的紧凑型基因组编辑工具
但即使是Cas9也有局限性。将遗传物质传递到宿主细胞的常用方法是使用修饰过的病毒作为载体。腺相关病毒(AAV)对患者无害,可以进入许多不同类型的细胞,引入Cas9等CRISPR酶,与其他一些方法相比,引发不良免疫反应的可能性较低。然而,像任何包裹递送服务一样,有尺寸限制。
东京大学生物科学系的Osamu Nureki教授解释说:“Cas9处于这种大小限制的极限,因此需要一种更小的Cas蛋白,可以有效地包装成AAV并作为基因组编辑工具。”
它的大尺寸意味着Cas9在用于基因治疗时可能缺乏效率。因此,一个大型的多机构团队致力于开发一种更小的Cas酶,它同样活跃,但效率更高。研究人员选择了一种名为AsCas12f的酶,这种酶来自于硫氧化轴二芽孢杆菌。这种酶的优点是它是迄今为止发现的最紧凑的Cas酶之一,其大小不到Cas9的三分之一。
新设计的CRISPR酶提供了一种更紧凑的DNA编辑解决方案,保持了现有工具的效率,并可以改善患者的治疗。新的基于CRISPR的基因编辑工具可能会为患有遗传性疾病的患者带来更好的治疗方法。这种工具是一种名为AsCas12f的酶,它经过了修饰,可以提供同样的效果,但大小只有通常用于基因编辑的Cas9酶的三分之一。紧凑的尺寸意味着更多的它可以被装入载体病毒并传递到活细胞中,使其更有效。
在之前的测试中,AsCas12f在人类细胞中几乎没有任何基因组活性。
研究人员创建了一个可能的AsCas12f突变库,然后将选择的突变组合在一起,设计出一种编辑能力比原始未突变型高10倍的AsCas12f酶。这种基因工程的AsCas12f已经在小鼠身上成功进行了测试,并有可能在未来用于新的、更有效的治疗方法。

图2 AsCas12f编辑工具的应用
“使用一种称为深度突变扫描的筛选方法,我们通过用所有生命所基于的所有20种氨基酸取代AsCas12f的每个氨基酸残基,组装了一个潜在的新候选者库。由此,我们确定了200多个增强基因组编辑活性的突变,”Nureki解释说。“基于从AsCas12f的结构分析中获得的见解,我们选择并结合这些增强活性的氨基酸突变来创建一个修饰的AsCas12f。与通常的AsCas12f类型相比,这种工程AsCas12f具有10倍以上的基因组编辑活性,并且与Cas9相当,同时保持更小的尺寸。”
该团队已经对AsCas12f系统进行了动物试验,将其与其他基因结合起来,并将其施用于活小鼠。直接对人体进行治疗比提取细胞、在实验室对其进行编辑、再将其植入患者体内更可取,后者更耗时、更昂贵。测试的成功表明,经过改造的AsCas12f具有用于人类基因治疗的潜力,例如治疗血友病(一种血液不能正常凝结的疾病)。
该团队发现了许多潜在的有效组合,用于设计改进的AsCas12f基因编辑系统,因此研究人员承认,选择的突变可能不是所有可用组合中最理想的。下一步,计算建模或机器学习可以用来筛选组合,并预测哪些可能会提供更好的改进。
“提升AsCas12f以展示与Cas9相当的基因组编辑活性是一项重大成就,并且是开发新的,更紧凑的基因组编辑工具的重要一步,”Nureki说。“对我们来说,基因疗法的关键在于它真正帮助病人的潜力。使用我们开发的工程AsCas12f,我们的下一个挑战是实际实施基因治疗,以帮助患有遗传疾病的人。”
参考资料
[1] An AsCas12f-based compact genome-editing tool derived by deep mutational scanning and structural analysis



