当前,心血管疾病致死率极高,正在导致全球医疗负担不断加重。在国家心血管病中心发布的《中国心血管健康与疾病报告2019》中,中国心血管病患病率处于持续上升阶段。根据推算,心血管病现患人数已达3.3亿,其中脑卒中1300万,冠心病 1100万,肺源性心脏病500万,心力衰竭890万,风湿性心脏病250万,先天性心脏病200万,下肢动脉疾病4530万,高血压2.45亿。中国心血管疾病已成为重大的公共卫生问题,防治心血管病刻不容缓。
而在心血管疾病中,心肌缺血再灌注损伤(Ischemia-reperfusion injury,IRI)是其发病和致死的主要危险因素之一。IRI是一个复杂的病理过程,当心脏冠状动脉发生急性梗阻,在一定时间内重新获得再通后,缺血的心肌得以恢复正常灌注,但是其梗阻期间的组织损伤反而会呈进行性加重,在心脏手术、心脏移植、心肌梗死和心脏骤停期间,对心脏造成损伤,甚至发生严重的心律失常而导致猝死。因此,对心肌缺血再灌注损伤的研究也成为了科学家们关注的重点。
尽管有数十年的研究和临床前数据作为基础,然而,目前没有药理学策略能够改善心肌缺血再灌注损伤的临床结果。直至近期,澳大利亚昆士兰大学的新研究又再次带来了新希望,其研究团队以 Therapeutic Inhibition of Acid Sensing Ion Channel 1a Recovers Heart Function After Ischemia-Reperfusion Injury 为题目,将新研究发布在杂志 Circulation 上,并以预印本的形式发于 bioRxiv 。
该项研究指出ACCN1基因的剪接变体ASIC1a(Acid Sensing Ion Channel 1a)是心肌缺血再灌注损伤反应的关键介质,而用漏斗网蜘蛛毒液中发现的衍生肽分子研制出的候选药物,可以防止心脏病发作造成的损害,并延长用于器官移植的供体心脏的寿命。

doi.org/10.1161/CIRCULATIONAHA.121.054360
在这项研究中,研究人员首先确认了ASIC1a在改善心肌缺血再灌注损伤方面的关键作用。他们使用CRISPR编辑来靶向ACCN1位点,敲除小鼠体内的ASIC1a,进行了特异性验证,对小鼠心脏进行Langendorff灌流并离体,从而评估心脏对IRI的耐受性。
为了评估对IRI的耐受性,研究人员对野生型(WT)和ASIC1a-KO两组小鼠同时进行了试验,对其心脏进行了25分钟的整体常温零流量缺血操作,接着进行45分钟的有氧再灌注。试验证明,再灌注期间,两组小鼠心脏的收缩功能随着时间的推移逐渐恢复,而ASIC1a-KO心脏的收缩恢复明显改善。这表明,ASIC1a在介导缺血诱导的神经元死亡中起到了关键作用,而通过基因消融或药物阻断抑制ASIC1a,将会对心肌缺血再灌注损伤的心脏具有神经保护作用。
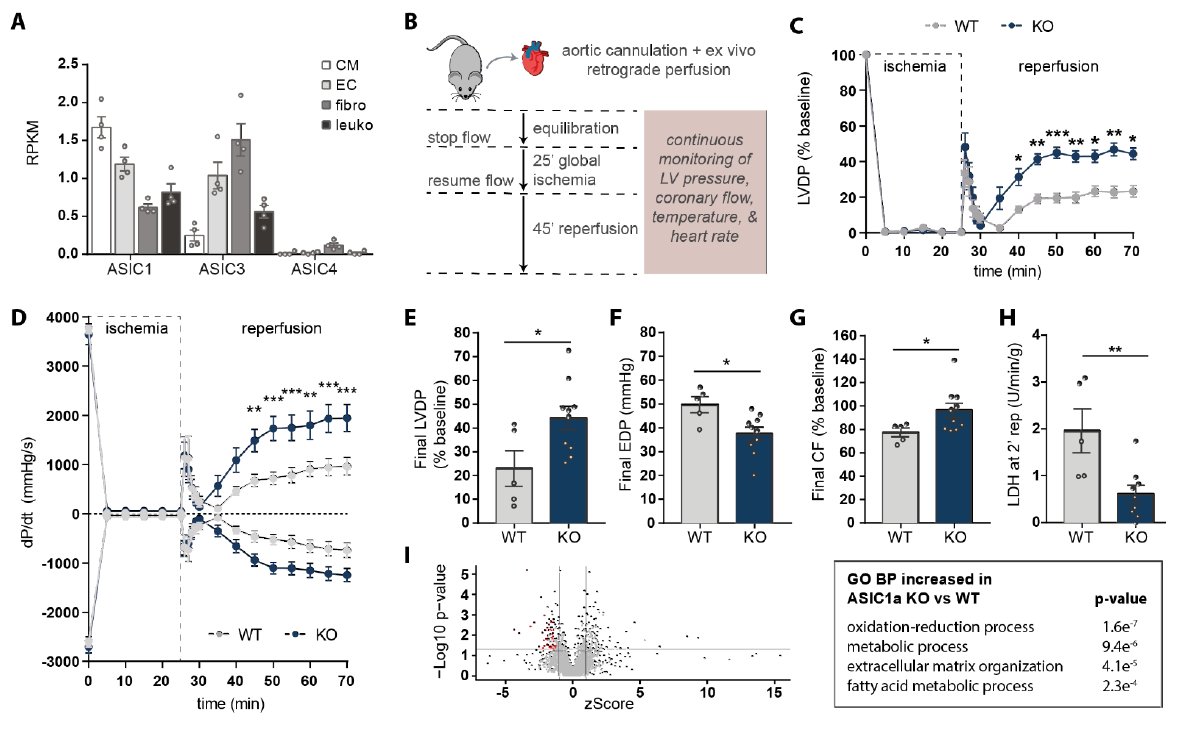
敲除ASIC1a基因后的小鼠心脏得到了更好的保护
由此,研究人员开始探究药物抑制ASIC1a是否具有保护心脏的作用,并选用了从澳大利亚漏斗网蜘蛛毒液中分离得到的一种双节肽Hi1a作为抑制剂,而Hi1a也是迄今为止鉴定过的较为有效的ASIC1a抑制剂。
研究人员在离体小鼠心脏冷藏8小时期间,用Hi1a制剂来补充标准临床心脏保存液,采用Langendorff逆行灌注法稳定心脏10分钟,然后将心脏转入工作模式,以评估生理负荷下的心功能。在评估基线血流动力学参数后,通过向冠状动脉循环中输注2–3°C的Celsior溶液阻止心脏跳动。心脏停搏后,心脏在低温条件下继续保存8小时,随后进行再灌注和功能分析。
得到的数据表明,添加Hi1a制剂进行保存的小鼠心脏主动脉流量和输出量的恢复明显改善,这证明,在临床相关的长时间冷藏供心保存模型中,Hi1a对IRI具有高度的心脏保护作用,同时,还可预防体内遭受心肌缺血再灌注损伤后的不良心室重构,并改善心脏功能。
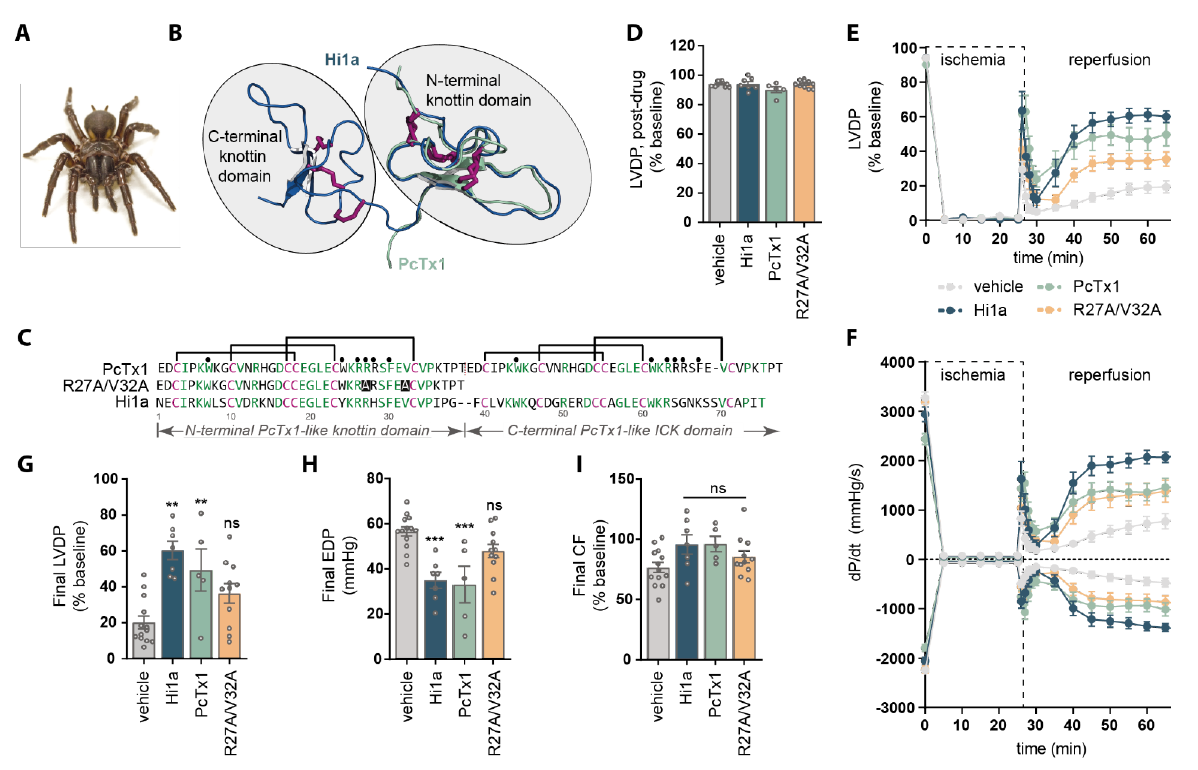
利用Hi1a研制而成的ASIC1a抑制剂改善并恢复了离体小鼠心脏遭受IRI后的心脏功能
在小鼠试验取得了理想效果后,研究人员将重点放在了ASIC1a在人类心脏中的表达。为了研究药物阻断ASIC1a是否对人体组织有治疗作用,他们使用了人诱导多能干细胞源性心肌细胞(hiPSC-CMs),其结果显示,ASIC1a会参与介导人心肌细胞的细胞死亡反应,同时,用Hi1a进行治疗可以保护心脏,其ASIC1a的药理学抑制对缺血诱导的细胞应激具有保护作用。
总的来说,ASIC1a靶向疗法在治疗心肌缺血再灌注损伤以及心脏移植应用中具有很大潜力,而在心血管领域,毒液衍生分子已被证明是一种创新疗法,此次的发现表明,ASIC1a抑制剂将有可能改善心血管疾病的公共卫生负担,并提升心脏缺血损伤患者的预后。



