摘要:一种罕见基因突变,可以使其携带者几乎无痛地生活,更快地愈合,并减少焦虑和恐惧。
伦敦大学学院的一项新研究揭示了一种罕见基因突变的生物学基础,这种突变可以使其携带者几乎无痛地生活,更快地愈合,并减少焦虑和恐惧。
这项研究发表在《大脑》杂志上,该研究小组在2019年发现了FAAH-OUT基因和罕见的突变,这种突变导致Jo Cameron几乎没有疼痛感,也从不感到焦虑或害怕。这项新研究描述了FAAH- out的突变如何“抑制”FAAH基因的表达,以及对与伤口愈合和情绪有关的其他分子途径的连锁反应。希望这些发现将导致新的药物靶点,并在这些领域开辟新的研究途径。

图1 新研究揭示了一种罕见基因突变的生物学基础
Jo Cameron住在苏格兰,2013年,她的医生注意到她在臀部和手部做了大手术后没有感到疼痛,于是她第一次被推荐给伦敦大学学院的疼痛遗传学家。经过六年的寻找,他们发现了一种新的基因,他们将其命名为FAAH-OUT,其中包含一种罕见的基因突变。与FAAH中另一种更常见的突变结合,发现它是Jo独特特征的原因。
基因组中含有FAAH- out的区域以前被认为是没有功能的“垃圾”dna,但它被发现可以调节FAAH的表达,FAAH是内源性大麻素系统的一部分,因其与疼痛、情绪和记忆有关而闻名。
在这项研究中,来自伦敦大学学院的研究小组试图了解FAAH-OUT在分子水平上是如何工作的,这是能够利用这种独特的生物学原理进行药物发现等应用的第一步。
这包括一系列方法,比如在细胞系上进行CRISPR-Cas9实验,模拟突变对其他基因的影响,以及分析基因的表达,看看哪些基因在与疼痛、情绪和愈合有关的分子途径中是活跃的。
研究小组观察到FAAH- out调节FAAH的表达。由于Jo Cameron携带的突变,FAAH酶活性水平显著降低。
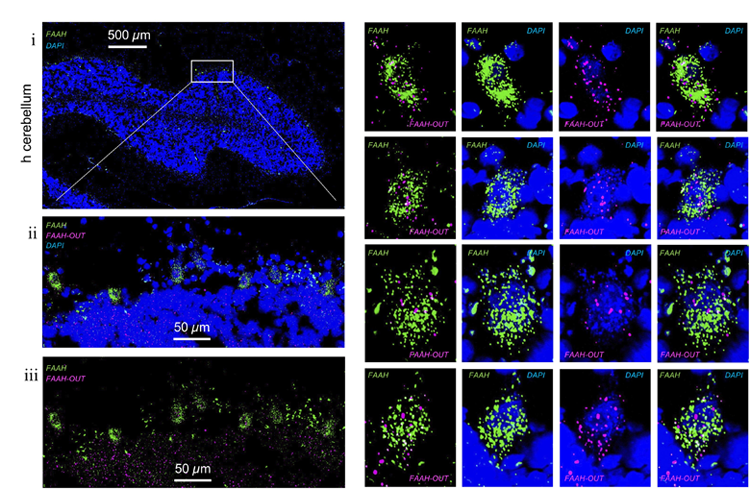
图2 FAAH和FAAH-OUT RNA在人脑组织细胞中的表达水平和定位
这项研究的资深作者Andrei Okorokov博士(伦敦大学学院医学院)说:“FAAH-OUT基因只是广袤大陆的一个小角落,这项研究已经开始绘制地图。”除了无痛的分子基础外,这些探索还确定了影响伤口愈合和情绪的分子途径,这些途径都受到FAAH-OUT突变的影响。作为科学家,我们有责任去探索,我认为这些发现将对伤口愈合、抑郁症等研究领域产生重要影响。”
作者观察了取自患者的成纤维细胞,以研究FAAH-OUT-FAAH轴对其他分子通路的影响。虽然乔·卡梅伦携带的基因突变可以抑制FAAH,但他们还发现了797个基因被激活,348个基因被抑制。这包括与伤口愈合相关的WNT通路的改变,以及先前与骨再生相关的WNT16基因活性的增加。
另外两个被改变的关键基因是BDNF和ACKR3,前者之前被认为与情绪调节有关,后者有助于调节阿片类药物的水平。这些基因变化可能导致乔·卡梅伦的焦虑、恐惧和痛苦程度较低。
James Cox 教授(伦敦大学学院医学院)是这项研究的资深作者,他说:“最初发现Jo独特表现型的遗传根源是一个令人兴奋的时刻,非常令人兴奋,但这些目前的发现才是真正开始变得有趣的地方。”通过精确地了解分子水平上发生的事情,我们可以开始了解所涉及的生物学,这为药物发现开辟了可能性,有朝一日可能对患者产生深远的积极影响。”
这项研究得到了医学研究委员会(MRC)和惠康基金会的支持。
注:所谓的“垃圾”DNA是指基因组中不产生蛋白质的区域或非编码基因。它们曾经被认为是多余的,但近年来,研究人员开始发现基因组的“暗”区域在调节编码基因中的作用。
参考资料:
[1] Molecular basis of FAAH-OUT-associated human pain insensitivity
摘要:一种罕见基因突变,可以使其携带者几乎无痛地生活,更快地愈合,并减少焦虑和恐惧。
伦敦大学学院的一项新研究揭示了一种罕见基因突变的生物学基础,这种突变可以使其携带者几乎无痛地生活,更快地愈合,并减少焦虑和恐惧。
这项研究发表在《大脑》杂志上,该研究小组在2019年发现了FAAH-OUT基因和罕见的突变,这种突变导致Jo Cameron几乎没有疼痛感,也从不感到焦虑或害怕。这项新研究描述了FAAH- out的突变如何“抑制”FAAH基因的表达,以及对与伤口愈合和情绪有关的其他分子途径的连锁反应。希望这些发现将导致新的药物靶点,并在这些领域开辟新的研究途径。

图1 新研究揭示了一种罕见基因突变的生物学基础
Jo Cameron住在苏格兰,2013年,她的医生注意到她在臀部和手部做了大手术后没有感到疼痛,于是她第一次被推荐给伦敦大学学院的疼痛遗传学家。经过六年的寻找,他们发现了一种新的基因,他们将其命名为FAAH-OUT,其中包含一种罕见的基因突变。与FAAH中另一种更常见的突变结合,发现它是Jo独特特征的原因。
基因组中含有FAAH- out的区域以前被认为是没有功能的“垃圾”dna,但它被发现可以调节FAAH的表达,FAAH是内源性大麻素系统的一部分,因其与疼痛、情绪和记忆有关而闻名。
在这项研究中,来自伦敦大学学院的研究小组试图了解FAAH-OUT在分子水平上是如何工作的,这是能够利用这种独特的生物学原理进行药物发现等应用的第一步。
这包括一系列方法,比如在细胞系上进行CRISPR-Cas9实验,模拟突变对其他基因的影响,以及分析基因的表达,看看哪些基因在与疼痛、情绪和愈合有关的分子途径中是活跃的。
研究小组观察到FAAH- out调节FAAH的表达。由于Jo Cameron携带的突变,FAAH酶活性水平显著降低。

图2 FAAH和FAAH-OUT RNA在人脑组织细胞中的表达水平和定位
这项研究的资深作者Andrei Okorokov博士(伦敦大学学院医学院)说:“FAAH-OUT基因只是广袤大陆的一个小角落,这项研究已经开始绘制地图。”除了无痛的分子基础外,这些探索还确定了影响伤口愈合和情绪的分子途径,这些途径都受到FAAH-OUT突变的影响。作为科学家,我们有责任去探索,我认为这些发现将对伤口愈合、抑郁症等研究领域产生重要影响。”
作者观察了取自患者的成纤维细胞,以研究FAAH-OUT-FAAH轴对其他分子通路的影响。虽然乔·卡梅伦携带的基因突变可以抑制FAAH,但他们还发现了797个基因被激活,348个基因被抑制。这包括与伤口愈合相关的WNT通路的改变,以及先前与骨再生相关的WNT16基因活性的增加。
另外两个被改变的关键基因是BDNF和ACKR3,前者之前被认为与情绪调节有关,后者有助于调节阿片类药物的水平。这些基因变化可能导致乔·卡梅伦的焦虑、恐惧和痛苦程度较低。
James Cox 教授(伦敦大学学院医学院)是这项研究的资深作者,他说:“最初发现Jo独特表现型的遗传根源是一个令人兴奋的时刻,非常令人兴奋,但这些目前的发现才是真正开始变得有趣的地方。”通过精确地了解分子水平上发生的事情,我们可以开始了解所涉及的生物学,这为药物发现开辟了可能性,有朝一日可能对患者产生深远的积极影响。”
这项研究得到了医学研究委员会(MRC)和惠康基金会的支持。
注:所谓的“垃圾”DNA是指基因组中不产生蛋白质的区域或非编码基因。它们曾经被认为是多余的,但近年来,研究人员开始发现基因组的“暗”区域在调节编码基因中的作用。
参考资料:
[1] Molecular basis of FAAH-OUT-associated human pain insensitivity



