摘要:当发现一个新的病例时,调查人员可以在它们之间建立联系,从而得出关于病因和治疗的更有力、更有说服力的想法。
一个病人可以引发新的研究问题,并提供有关疾病的答案。当发现一个新的病例时,调查人员可以在它们之间建立联系,从而得出关于病因和治疗的更有力、更有说服力的想法。今天在《自然医学》杂志上发表的一篇文章中,由麻省总医院(MGH)和大众眼耳医院(Mass Eye and Ear)两家布里格姆医院的研究人员领导的一个国际研究小组报告了一个新病例,该患者具有早发性阿尔茨海默病的遗传易感性,但直到60多岁,他的认知能力仍然完好无损。通过由哥伦比亚安蒂奥基亚大学的研究人员领导的临床评估,在Mass Eye and Ear和洛杉矶儿童医院进行的遗传和分子研究,在MGH进行的神经成像和生物标志物研究,以及由德国汉堡-埃本多夫大学医学中心的研究人员进行的神经病理学研究,研究小组确定了一种新的基因变异,可以预防阿尔茨海默病。该变异发生在与2019年报道的同一家族病例不同的基因上,但指出了一种共同的疾病途径。他们的发现还指出了大脑的一个区域,这个区域可能在未来提供最佳的治疗目标。

图1 研究小组确定了一种新的基因变异,可以预防阿尔茨海默病
“我们已经确定的基因变异指向了一条途径,它可以产生极端的弹性,并保护人们免受阿尔茨海默病的症状,”Joseph F. Arboleda-Velasquez博士说。“没有病人,我们就无法获得这些见解。他们向我们展示了在保护方面什么是重要的,并挑战了该领域关于阿尔茨海默病及其进展的许多假设。”
引起调查人员注意的案件涉及世界上已知最大的亲属的一个家庭成员,他的基因变异被称为“Paisa”突变(早老素-1 E280A)。这种变异的携带者通常在44岁时出现轻度认知障碍,49岁时出现痴呆,60多岁时死于痴呆并发症。弗朗西斯科·洛佩拉,医学博士,哥伦比亚Medellín安蒂奥基亚神经科学小组主任,自然医学论文的第一作者之一,是发现这个家族的神经学家,并在过去的30年里一直在跟踪他们。这组调查人员之前研究了这个家庭的一名妇女,她直到70多岁都没有受伤,她的病例于2019年被报道。在他们最新发表的《自然医学》(Nature Medicine)论文中,研究人员描述了一名携带Paisa突变基因的男性患者,他的认知能力一直保持完整,直到67岁。他在72岁时患上了轻度痴呆,74岁时去世——比大多数携带Paisa基因突变的人晚了几十年。
“像这样的特殊案例说明了患有阿尔茨海默病的个人和大家庭如何帮助我们提高对这种疾病的理解,并为发现开辟新的途径,”共同资深作者Yakeel T. Quiroz博士说,“我们从第二个病例中获得的见解可能会指导我们在大脑中我们需要寻找延缓和阻止疾病进展的地方,并将帮助我们对可能导致阿尔茨海默氏症痴呆症的一系列步骤形成新的假设。”
“我们在研究这两个受保护的案例时所做的就是解读大自然,最令人兴奋的是,大自然向我们揭示了老年痴呆症的病因和治疗方法。大自然母亲对这两位受试者做了一项特殊的实验:她赋予他们一种导致阿尔茨海默氏症的基因,同时赋予另一种基因,使他们在20多年的时间里免受这种疾病的症状影响。因此,解决方案是通过开发治疗方法来模仿自然,模仿这些基因变异对有患病风险的受试者的保护机制。”
“为预防和治疗不治之症打开了一扇大门。”
这名男性患者参加了麻省总医院哥伦比亚-波士顿生物标志物研究(COLBOS),该研究将6000名已知Paisa突变的大家庭成员带到波士顿进行高级神经成像、生物标志物和基因检查。同样的研究之前发现了一个病例,一位女性患者携带了两份罕见的克赖斯特彻奇基因变异,这种变异会影响APOE3——一种与阿尔茨海默病密切相关的蛋白质。然而,研究人员排除了在男性患者中存在APOE克赖斯特彻奇基因变异的可能性。该团队与洛杉矶儿童医院的Xiaowu Gai博士和同事合作,在Mass Eye and Ear进行了遗传和分子分析,以确定可能保护他免受阿尔茨海默病的其他变异。最有希望的候选者是一个新的和罕见的变异,以前从未报道过Reelin基因。该团队将其命名为Reelin-COLBOS。在共同资深作者Diego Sepulveda-Falla博士领导的研究中,他是汉堡-埃彭多夫大学医学中心神经病理学研究所的首席研究员,研究小组进一步验证了Reelin-COLBOS变异在小鼠模型和神经病理学研究中的保护作用。
Sepulveda-Falla说:“每个受保护的病例,APOE克赖斯特彻奇病例和rerin - colbos病例,在尸检分析中都显示出一种独特的保护模式,一种是全球性的,另一种是地方性的。”“这些杰出的案例告诉我们,阿尔茨海默氏症的保护可以采取不同的形式,也许一种治疗方法可以通过针对关键的大脑结构,如内嗅皮层,取得成功。”它们迫使我们修改我们以前关于神经退化和认知能力下降的概念。这对我们来说是激动人心的时刻,希望对阿尔茨海默病研究领域也是如此。”
研究人员将Reelin描述为更著名的APOE的“表亲”。Reelin和APOE都竞争结合到相似的细胞受体上,本质上是争夺同一位置。当Reelin位于受体位置时,它会减少tau蛋白的磷酸化,这种蛋白在阿尔茨海默病患者的大脑中形成病理缠结。当APOE与受体结合时,它会产生相反的效果。
Reelin是一种在脑细胞发育和功能调节中起关键作用的蛋白质。事实上,之前的报告已经将Reelin突变与自闭症、精神分裂症、癫痫和双相情感障碍等疾病联系起来。然而,与疾病相关的突变是不同的,因为它们减少了蛋白质的功能,而在Reelin-COLBOS的情况下,保护性变异增加了蛋白质的功能。
“当我们看到这种变异的最佳候选者之一坐在雷林时,有点震惊。”“第一个病例向我们展示了一种影响APOE的变异,第二个病例影响Reelin,这一事实告诉我们,这种控制tau磷酸化的信号通路,以及其他影响,可能是理解为什么这些患者受到保护的关键。这对指导治疗至关重要,因为它清楚地告诉我们,更多的Reelin可能有潜在的有益效果。”
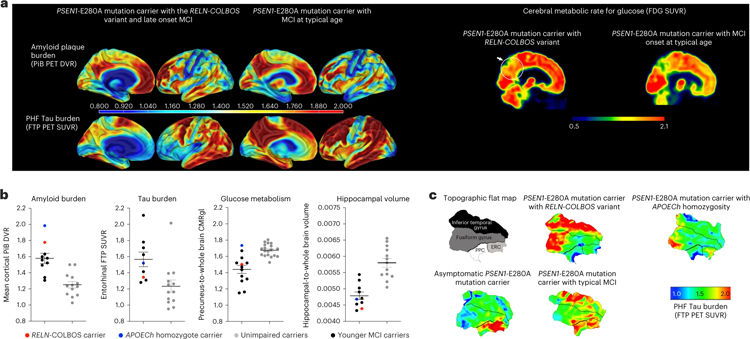
图2 RELN-COLBOS(H3447R)载体的PET成像
最近的一位患者在73岁时在马萨诸塞州总医院接受了神经影像学检查。这些扫描显示,虽然患者的淀粉样β斑块负担很高,并且他的大脑某些区域有tau缠结,但他的内嗅皮层有非常有限的tau病理学。内嗅皮层在记忆和学习中起着至关重要的作用,它的退化会导致认知障碍和痴呆。在小鼠模型中的研究也表明,Reelin-COLBOS变体可以防止tau病理。
Quiroz说:“这个病例表明,内嗅区可能代表了一个对预防痴呆症至关重要的小目标。”
随着研究人员追求基因疗法,未来可能会提供可以修改或操纵基因表达的治疗方法,了解大脑的哪个区域将会变得越来越重要。
许多治疗阿尔茨海默病的药物,包括最近被美国食品和药物管理局批准的药物,以及目前正在临床试验的其他药物,都旨在减少淀粉样斑块的形成。这项研究的结果指出了潜在的新治疗途径,因为这两名接受保护的患者的大脑中淀粉样蛋白水平极高,但他们还是受到了保护。
“这些令人兴奋的发现证明了学术合作的力量,视网膜疾病遗传学专家与当地神经影像学权威机构合作,可以与世界各地领先的神经学家和神经病理学家合作,以推动科学发现,”Joan W. Miller医学博士,“阿尔茨海默病仍然是一种毁灭性的疾病,给全球带来了巨大的负担,这项工作为进一步研究这种恢复途径如何导致有效的治疗策略打开了大门。”
研究人员指出,他们不能完全排除其他因素,包括额外的基因变异,可能有助于患者对阿尔茨海默病症状的抵抗力。但他们在临床前研究中的实验证据强烈暗示了Reelin-COLBOS变体。
Arboleda-Velasquez和Quiroz与Lopera和Sepulveda-Falla一起,计划继续开展工作,从这些哥伦比亚家庭中确定更多受保护的患者,并从每个特殊病例中学习。他们也在研究针对这一保护性途径的治疗方法。
参考资料:
[1] Resilience to autosomal dominant Alzheimer’s disease in a Reelin-COLBOS heterozygous man
摘要:当发现一个新的病例时,调查人员可以在它们之间建立联系,从而得出关于病因和治疗的更有力、更有说服力的想法。
一个病人可以引发新的研究问题,并提供有关疾病的答案。当发现一个新的病例时,调查人员可以在它们之间建立联系,从而得出关于病因和治疗的更有力、更有说服力的想法。今天在《自然医学》杂志上发表的一篇文章中,由麻省总医院(MGH)和大众眼耳医院(Mass Eye and Ear)两家布里格姆医院的研究人员领导的一个国际研究小组报告了一个新病例,该患者具有早发性阿尔茨海默病的遗传易感性,但直到60多岁,他的认知能力仍然完好无损。通过由哥伦比亚安蒂奥基亚大学的研究人员领导的临床评估,在Mass Eye and Ear和洛杉矶儿童医院进行的遗传和分子研究,在MGH进行的神经成像和生物标志物研究,以及由德国汉堡-埃本多夫大学医学中心的研究人员进行的神经病理学研究,研究小组确定了一种新的基因变异,可以预防阿尔茨海默病。该变异发生在与2019年报道的同一家族病例不同的基因上,但指出了一种共同的疾病途径。他们的发现还指出了大脑的一个区域,这个区域可能在未来提供最佳的治疗目标。

图1 研究小组确定了一种新的基因变异,可以预防阿尔茨海默病
“我们已经确定的基因变异指向了一条途径,它可以产生极端的弹性,并保护人们免受阿尔茨海默病的症状,”Joseph F. Arboleda-Velasquez博士说。“没有病人,我们就无法获得这些见解。他们向我们展示了在保护方面什么是重要的,并挑战了该领域关于阿尔茨海默病及其进展的许多假设。”
引起调查人员注意的案件涉及世界上已知最大的亲属的一个家庭成员,他的基因变异被称为“Paisa”突变(早老素-1 E280A)。这种变异的携带者通常在44岁时出现轻度认知障碍,49岁时出现痴呆,60多岁时死于痴呆并发症。弗朗西斯科·洛佩拉,医学博士,哥伦比亚Medellín安蒂奥基亚神经科学小组主任,自然医学论文的第一作者之一,是发现这个家族的神经学家,并在过去的30年里一直在跟踪他们。这组调查人员之前研究了这个家庭的一名妇女,她直到70多岁都没有受伤,她的病例于2019年被报道。在他们最新发表的《自然医学》(Nature Medicine)论文中,研究人员描述了一名携带Paisa突变基因的男性患者,他的认知能力一直保持完整,直到67岁。他在72岁时患上了轻度痴呆,74岁时去世——比大多数携带Paisa基因突变的人晚了几十年。
“像这样的特殊案例说明了患有阿尔茨海默病的个人和大家庭如何帮助我们提高对这种疾病的理解,并为发现开辟新的途径,”共同资深作者Yakeel T. Quiroz博士说,“我们从第二个病例中获得的见解可能会指导我们在大脑中我们需要寻找延缓和阻止疾病进展的地方,并将帮助我们对可能导致阿尔茨海默氏症痴呆症的一系列步骤形成新的假设。”
“我们在研究这两个受保护的案例时所做的就是解读大自然,最令人兴奋的是,大自然向我们揭示了老年痴呆症的病因和治疗方法。大自然母亲对这两位受试者做了一项特殊的实验:她赋予他们一种导致阿尔茨海默氏症的基因,同时赋予另一种基因,使他们在20多年的时间里免受这种疾病的症状影响。因此,解决方案是通过开发治疗方法来模仿自然,模仿这些基因变异对有患病风险的受试者的保护机制。”
“为预防和治疗不治之症打开了一扇大门。”
这名男性患者参加了麻省总医院哥伦比亚-波士顿生物标志物研究(COLBOS),该研究将6000名已知Paisa突变的大家庭成员带到波士顿进行高级神经成像、生物标志物和基因检查。同样的研究之前发现了一个病例,一位女性患者携带了两份罕见的克赖斯特彻奇基因变异,这种变异会影响APOE3——一种与阿尔茨海默病密切相关的蛋白质。然而,研究人员排除了在男性患者中存在APOE克赖斯特彻奇基因变异的可能性。该团队与洛杉矶儿童医院的Xiaowu Gai博士和同事合作,在Mass Eye and Ear进行了遗传和分子分析,以确定可能保护他免受阿尔茨海默病的其他变异。最有希望的候选者是一个新的和罕见的变异,以前从未报道过Reelin基因。该团队将其命名为Reelin-COLBOS。在共同资深作者Diego Sepulveda-Falla博士领导的研究中,他是汉堡-埃彭多夫大学医学中心神经病理学研究所的首席研究员,研究小组进一步验证了Reelin-COLBOS变异在小鼠模型和神经病理学研究中的保护作用。
Sepulveda-Falla说:“每个受保护的病例,APOE克赖斯特彻奇病例和rerin - colbos病例,在尸检分析中都显示出一种独特的保护模式,一种是全球性的,另一种是地方性的。”“这些杰出的案例告诉我们,阿尔茨海默氏症的保护可以采取不同的形式,也许一种治疗方法可以通过针对关键的大脑结构,如内嗅皮层,取得成功。”它们迫使我们修改我们以前关于神经退化和认知能力下降的概念。这对我们来说是激动人心的时刻,希望对阿尔茨海默病研究领域也是如此。”
研究人员将Reelin描述为更著名的APOE的“表亲”。Reelin和APOE都竞争结合到相似的细胞受体上,本质上是争夺同一位置。当Reelin位于受体位置时,它会减少tau蛋白的磷酸化,这种蛋白在阿尔茨海默病患者的大脑中形成病理缠结。当APOE与受体结合时,它会产生相反的效果。
Reelin是一种在脑细胞发育和功能调节中起关键作用的蛋白质。事实上,之前的报告已经将Reelin突变与自闭症、精神分裂症、癫痫和双相情感障碍等疾病联系起来。然而,与疾病相关的突变是不同的,因为它们减少了蛋白质的功能,而在Reelin-COLBOS的情况下,保护性变异增加了蛋白质的功能。
“当我们看到这种变异的最佳候选者之一坐在雷林时,有点震惊。”“第一个病例向我们展示了一种影响APOE的变异,第二个病例影响Reelin,这一事实告诉我们,这种控制tau磷酸化的信号通路,以及其他影响,可能是理解为什么这些患者受到保护的关键。这对指导治疗至关重要,因为它清楚地告诉我们,更多的Reelin可能有潜在的有益效果。”

图2 RELN-COLBOS(H3447R)载体的PET成像
最近的一位患者在73岁时在马萨诸塞州总医院接受了神经影像学检查。这些扫描显示,虽然患者的淀粉样β斑块负担很高,并且他的大脑某些区域有tau缠结,但他的内嗅皮层有非常有限的tau病理学。内嗅皮层在记忆和学习中起着至关重要的作用,它的退化会导致认知障碍和痴呆。在小鼠模型中的研究也表明,Reelin-COLBOS变体可以防止tau病理。
Quiroz说:“这个病例表明,内嗅区可能代表了一个对预防痴呆症至关重要的小目标。”
随着研究人员追求基因疗法,未来可能会提供可以修改或操纵基因表达的治疗方法,了解大脑的哪个区域将会变得越来越重要。
许多治疗阿尔茨海默病的药物,包括最近被美国食品和药物管理局批准的药物,以及目前正在临床试验的其他药物,都旨在减少淀粉样斑块的形成。这项研究的结果指出了潜在的新治疗途径,因为这两名接受保护的患者的大脑中淀粉样蛋白水平极高,但他们还是受到了保护。
“这些令人兴奋的发现证明了学术合作的力量,视网膜疾病遗传学专家与当地神经影像学权威机构合作,可以与世界各地领先的神经学家和神经病理学家合作,以推动科学发现,”Joan W. Miller医学博士,“阿尔茨海默病仍然是一种毁灭性的疾病,给全球带来了巨大的负担,这项工作为进一步研究这种恢复途径如何导致有效的治疗策略打开了大门。”
研究人员指出,他们不能完全排除其他因素,包括额外的基因变异,可能有助于患者对阿尔茨海默病症状的抵抗力。但他们在临床前研究中的实验证据强烈暗示了Reelin-COLBOS变体。
Arboleda-Velasquez和Quiroz与Lopera和Sepulveda-Falla一起,计划继续开展工作,从这些哥伦比亚家庭中确定更多受保护的患者,并从每个特殊病例中学习。他们也在研究针对这一保护性途径的治疗方法。
参考资料:
[1] Resilience to autosomal dominant Alzheimer’s disease in a Reelin-COLBOS heterozygous man



