摘要:抗生素有助于对抗细菌感染,但它们也会伤害生活在肠道中的有益微生物,这可能会对健康产生长期的影响。欧洲临床微生物学与传染病大会(ECCMID)上发表的一项新研究确定了几种保护性药物,可能会减轻抗生素造成的附带损害,而不会影响它们对有害细菌的有效性。
抗生素有助于对抗细菌感染,但它们也会伤害生活在肠道中的有益微生物,这可能会对健康产生长期的影响。
在今年于丹麦哥本哈根(4月15-18日)举行的欧洲临床微生物学与传染病大会(ECCMID)上发表的一项新研究确定了几种保护性药物,这些药物可能会减轻抗生素造成的附带损害,而不会影响它们对有害细菌的有效性。
德国海德堡欧洲分子生物学实验室的Lisa Maier博士和Camille V. Goemans博士及其同事进行了一项独特的研究,分析了144种不同抗生素对最常见肠道细菌丰度的影响,为减少抗生素治疗对肠道微生物组的不良影响提供了新的见解。
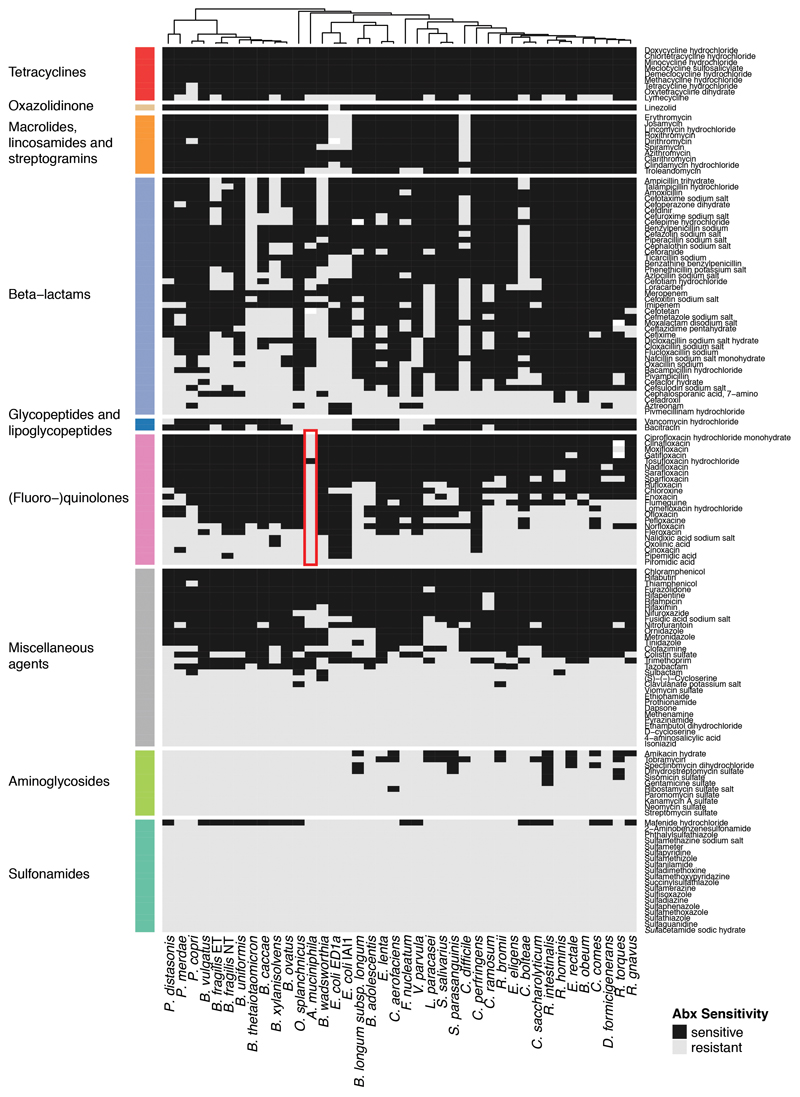
图1 144种抗生素对40种人类肠道共生菌的影响
人体肠道中的数万亿微生物通过帮助消化、提供营养物质和代谢物,以及与免疫系统一起抵御有害细菌和病毒,对健康产生了深远的影响。
抗生素会破坏这些微生物群落,导致不平衡,从而导致艰难梭菌感染引起的反复胃肠道问题,以及肥胖、过敏、哮喘和其他免疫或炎症性疾病等长期健康问题。
尽管有这种众所周知的附带损害,但由于技术挑战,哪些抗生素会影响哪种细菌种类,以及这些负面副作用是否会得到缓解,还没有进行系统的研究。
为了了解更多,研究人员系统地分析了在144种不同抗生素治疗后,肠道中常见的27种不同细菌的生长和存活情况。他们还评估了800多种抗生素-细菌组合的最低抑制浓度(MIC)——阻止细菌生长所需的抗生素的最低浓度。
结果显示,大多数肠道细菌的mic略高于致病细菌,这表明在常用抗生素浓度下,大多数测试的肠道细菌不会受到影响。
然而,两种广泛使用的抗生素——四环素类和大环内酯类——不仅以远低于阻止致病细菌生长所需浓度的浓度阻止了健康细菌的生长,而且还杀死了他们测试的一半以上的肠道细菌物种,可能会在很长一段时间内改变肠道微生物组的组成。
由于药物在不同细菌物种之间的相互作用不同,研究人员调查了是否可以使用第二种药物来保护肠道微生物。他们将抗生素红霉素(一种大环内酯)和强力霉素(一种四环素)与一套1197种药物结合起来,以确定合适的药物,可以保护两种丰富的肠道细菌(普通杆菌和均匀杆菌)免受抗生素的侵害。
研究人员发现了几种有前景的药物,包括抗凝血剂双苦马酚,痛风药物苯溴马隆,以及两种消炎药,托芬那酸和二氟尼拉。
重要的是,这些药物并没有影响抗生素对抗致病细菌的效果。
进一步的实验表明,这些解毒剂还可以保护来自人类粪便样本和活小鼠的天然细菌群落。
德国柏林分子医学的Ulrike Lber博士在ECCMID上介绍了这项研究,他说:“一个国际科学家团队的这项艰巨任务已经确定了一种新的方法,将抗生素与保护性解毒剂结合起来,帮助保持肠道微生物群的健康,并在不影响抗生素效率的情况下减少抗生素的有害副作用。”“尽管我们的发现很有希望,但还需要进一步的研究来确定最佳和个性化的解毒剂组合,并排除对肠道微生物组的任何潜在的长期影响。”
参考资料:
[1] Study offers novel insights into reducing adverse effects of antibiotics on the gut microbiome
摘要:抗生素有助于对抗细菌感染,但它们也会伤害生活在肠道中的有益微生物,这可能会对健康产生长期的影响。欧洲临床微生物学与传染病大会(ECCMID)上发表的一项新研究确定了几种保护性药物,可能会减轻抗生素造成的附带损害,而不会影响它们对有害细菌的有效性。
抗生素有助于对抗细菌感染,但它们也会伤害生活在肠道中的有益微生物,这可能会对健康产生长期的影响。
在今年于丹麦哥本哈根(4月15-18日)举行的欧洲临床微生物学与传染病大会(ECCMID)上发表的一项新研究确定了几种保护性药物,这些药物可能会减轻抗生素造成的附带损害,而不会影响它们对有害细菌的有效性。
德国海德堡欧洲分子生物学实验室的Lisa Maier博士和Camille V. Goemans博士及其同事进行了一项独特的研究,分析了144种不同抗生素对最常见肠道细菌丰度的影响,为减少抗生素治疗对肠道微生物组的不良影响提供了新的见解。

图1 144种抗生素对40种人类肠道共生菌的影响
人体肠道中的数万亿微生物通过帮助消化、提供营养物质和代谢物,以及与免疫系统一起抵御有害细菌和病毒,对健康产生了深远的影响。
抗生素会破坏这些微生物群落,导致不平衡,从而导致艰难梭菌感染引起的反复胃肠道问题,以及肥胖、过敏、哮喘和其他免疫或炎症性疾病等长期健康问题。
尽管有这种众所周知的附带损害,但由于技术挑战,哪些抗生素会影响哪种细菌种类,以及这些负面副作用是否会得到缓解,还没有进行系统的研究。
为了了解更多,研究人员系统地分析了在144种不同抗生素治疗后,肠道中常见的27种不同细菌的生长和存活情况。他们还评估了800多种抗生素-细菌组合的最低抑制浓度(MIC)——阻止细菌生长所需的抗生素的最低浓度。
结果显示,大多数肠道细菌的mic略高于致病细菌,这表明在常用抗生素浓度下,大多数测试的肠道细菌不会受到影响。
然而,两种广泛使用的抗生素——四环素类和大环内酯类——不仅以远低于阻止致病细菌生长所需浓度的浓度阻止了健康细菌的生长,而且还杀死了他们测试的一半以上的肠道细菌物种,可能会在很长一段时间内改变肠道微生物组的组成。
由于药物在不同细菌物种之间的相互作用不同,研究人员调查了是否可以使用第二种药物来保护肠道微生物。他们将抗生素红霉素(一种大环内酯)和强力霉素(一种四环素)与一套1197种药物结合起来,以确定合适的药物,可以保护两种丰富的肠道细菌(普通杆菌和均匀杆菌)免受抗生素的侵害。
研究人员发现了几种有前景的药物,包括抗凝血剂双苦马酚,痛风药物苯溴马隆,以及两种消炎药,托芬那酸和二氟尼拉。
重要的是,这些药物并没有影响抗生素对抗致病细菌的效果。
进一步的实验表明,这些解毒剂还可以保护来自人类粪便样本和活小鼠的天然细菌群落。
德国柏林分子医学的Ulrike Lber博士在ECCMID上介绍了这项研究,他说:“一个国际科学家团队的这项艰巨任务已经确定了一种新的方法,将抗生素与保护性解毒剂结合起来,帮助保持肠道微生物群的健康,并在不影响抗生素效率的情况下减少抗生素的有害副作用。”“尽管我们的发现很有希望,但还需要进一步的研究来确定最佳和个性化的解毒剂组合,并排除对肠道微生物组的任何潜在的长期影响。”
参考资料:
[1] Study offers novel insights into reducing adverse effects of antibiotics on the gut microbiome



