摘要:科学家们首次使用CRISPR技术插入基因,使免疫细胞集中攻击癌细胞,有可能使正常细胞不受伤害,并提高免疫治疗的有效性。
科学家首次使用CRISPR技术插入基因,使免疫细胞集中攻击癌细胞,有可能使正常细胞不受伤害,并提高免疫治疗的有效性。新方法在癌症免疫治疗学会(SITC) 2022上发表,并发表在《自然》杂志上。该研究由UCLA Jonsson综合癌症中心的Antoni Ribas医学博士和UCLA医学教授共同领导。

图1 科学家首次使用CRISPR技术插入基因使免疫细胞集中攻击癌细胞(图源:[1])
CRISPR技术以前曾被用于去除人类的特定基因,使免疫系统更活跃地对抗癌症。在这项新研究中,PACT制药公司的研究人员报告称,他们不仅能够使用CRISPR去除特定基因,还能在免疫细胞中插入新的基因,有效地重新定向免疫细胞,识别患者自身癌细胞的突变。当注入回患者体内时,这些CRISPR工程免疫细胞优先流向癌细胞,并成为那里最有代表性的免疫细胞。
这项新研究报告了一种从患者自身血液中分离免疫受体的有效方法,使用的新技术最初是由Ribas博士与西雅图系统生物学研究所所长James Heath博士、诺贝尔奖得主David Baltimore博士、加州理工学院名誉教授和UCLA Jonsson综合癌症中心成员合作开发的,并由PACT制药公司进一步发展到临床。分离后,利用CRISPR基因编辑,免疫受体被用于重定向免疫细胞来识别癌症。
“这是在开发癌症个性化治疗方面的一个飞跃,在这种治疗中,专门识别患者自身癌症突变的免疫受体被用来治疗癌症。”该文章的通讯作者Ribas博士说。“如果没有新开发的CRISPR技术一步取代临床级细胞制剂中的免疫受体的能力,就不可能产生针对癌症的个性化细胞治疗方法。”
研究人员报告说,他们治疗了16名患有各种实体癌症的患者,包括结肠癌、乳腺癌和肺癌。根据结合情况,从患者的血液中分离出免疫细胞,以捕获从患者自身癌症中显示出350个突变的试剂,针对免疫系统34种HLA亚型的总共超过5000个突变。让免疫细胞特异性识别癌症突变的免疫受体的基因被测序,总共有175个新分离的癌症特异性免疫受体。然后,通过一步式CRISPR编辑,它们被插入到患者自身的免疫细胞中,这包括敲除现有的免疫细胞受体和敲入可以重定向这些细胞以专门识别癌症突变的免疫受体。
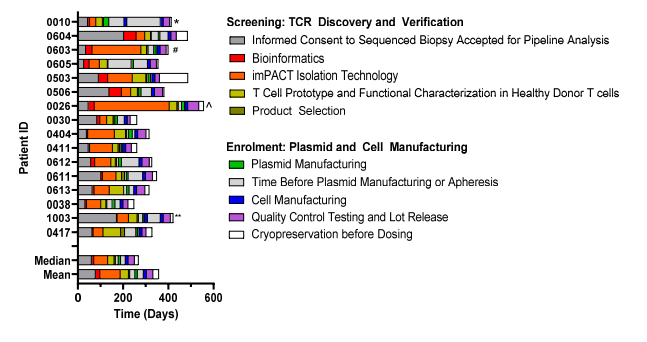
图2 最终接受治疗的14名患者筛选和给药之间的时间线(图源:[1])
在给予条件性化疗后,多达三种这样的基因编辑免疫细胞被注入回患者体内,参与这项研究的16名患者共被注入37种免疫受体。患者出现了化疗的预期副作用,两名患者出现了基因编辑细胞的潜在副作用,一名患者出现发烧和发冷,另一名患者出现精神错乱,两名患者都迅速康复。基因编辑的免疫细胞优先从患者输注后的活组织检查中恢复,通常代表癌症中前20%的免疫细胞。
“这项研究证明了分离和克隆多个识别癌细胞突变的免疫细胞受体的可行性,使用单步、非病毒精确基因组编辑同时敲除内源性免疫受体和敲入重定向免疫受体的可行性,制造临床级别的CRISPR工程T细胞,注入多达三种基因编辑免疫细胞产品的安全性,以及基因编辑的免疫细胞运输到患者肿瘤的能力,”Ribas博士说。
参考资料:
[1] Non-viral precision T cell receptor replacement for personalized cell therapy
摘要:科学家们首次使用CRISPR技术插入基因,使免疫细胞集中攻击癌细胞,有可能使正常细胞不受伤害,并提高免疫治疗的有效性。
科学家首次使用CRISPR技术插入基因,使免疫细胞集中攻击癌细胞,有可能使正常细胞不受伤害,并提高免疫治疗的有效性。新方法在癌症免疫治疗学会(SITC) 2022上发表,并发表在《自然》杂志上。该研究由UCLA Jonsson综合癌症中心的Antoni Ribas医学博士和UCLA医学教授共同领导。

图1 科学家首次使用CRISPR技术插入基因使免疫细胞集中攻击癌细胞(图源:[1])
CRISPR技术以前曾被用于去除人类的特定基因,使免疫系统更活跃地对抗癌症。在这项新研究中,PACT制药公司的研究人员报告称,他们不仅能够使用CRISPR去除特定基因,还能在免疫细胞中插入新的基因,有效地重新定向免疫细胞,识别患者自身癌细胞的突变。当注入回患者体内时,这些CRISPR工程免疫细胞优先流向癌细胞,并成为那里最有代表性的免疫细胞。
这项新研究报告了一种从患者自身血液中分离免疫受体的有效方法,使用的新技术最初是由Ribas博士与西雅图系统生物学研究所所长James Heath博士、诺贝尔奖得主David Baltimore博士、加州理工学院名誉教授和UCLA Jonsson综合癌症中心成员合作开发的,并由PACT制药公司进一步发展到临床。分离后,利用CRISPR基因编辑,免疫受体被用于重定向免疫细胞来识别癌症。
“这是在开发癌症个性化治疗方面的一个飞跃,在这种治疗中,专门识别患者自身癌症突变的免疫受体被用来治疗癌症。”该文章的通讯作者Ribas博士说。“如果没有新开发的CRISPR技术一步取代临床级细胞制剂中的免疫受体的能力,就不可能产生针对癌症的个性化细胞治疗方法。”
研究人员报告说,他们治疗了16名患有各种实体癌症的患者,包括结肠癌、乳腺癌和肺癌。根据结合情况,从患者的血液中分离出免疫细胞,以捕获从患者自身癌症中显示出350个突变的试剂,针对免疫系统34种HLA亚型的总共超过5000个突变。让免疫细胞特异性识别癌症突变的免疫受体的基因被测序,总共有175个新分离的癌症特异性免疫受体。然后,通过一步式CRISPR编辑,它们被插入到患者自身的免疫细胞中,这包括敲除现有的免疫细胞受体和敲入可以重定向这些细胞以专门识别癌症突变的免疫受体。

图2 最终接受治疗的14名患者筛选和给药之间的时间线(图源:[1])
在给予条件性化疗后,多达三种这样的基因编辑免疫细胞被注入回患者体内,参与这项研究的16名患者共被注入37种免疫受体。患者出现了化疗的预期副作用,两名患者出现了基因编辑细胞的潜在副作用,一名患者出现发烧和发冷,另一名患者出现精神错乱,两名患者都迅速康复。基因编辑的免疫细胞优先从患者输注后的活组织检查中恢复,通常代表癌症中前20%的免疫细胞。
“这项研究证明了分离和克隆多个识别癌细胞突变的免疫细胞受体的可行性,使用单步、非病毒精确基因组编辑同时敲除内源性免疫受体和敲入重定向免疫受体的可行性,制造临床级别的CRISPR工程T细胞,注入多达三种基因编辑免疫细胞产品的安全性,以及基因编辑的免疫细胞运输到患者肿瘤的能力,”Ribas博士说。
参考资料:
[1] Non-viral precision T cell receptor replacement for personalized cell therapy



