摘要:圣犹大儿童研究医院的科学家们发现,细胞对低氧的反应也会增加成人胎儿血红蛋白的表达,这可能会导致一些常见遗传性贫血的新疗法。
圣犹大儿童研究医院(St. Jude Children’s Research Hospital)的科学家已经展示了一种负责适应低氧环境(缺氧)的蛋白质是如何导致成人胎儿血红蛋白(HbF)表达增加的。这一发现对治疗镰状细胞病和乙型地中海贫血有一定的意义,这两种严重的血液疾病影响着数百万人。这项研究发表在今天的《Nature》。

图1 研究发现适应低氧环境的蛋白质是如何导致成人胎儿血红蛋白(HbF)表达增加(图源:[1])
血红蛋白就像一块蛋白质海绵,它能吸收氧气,并允许红血球将氧气运送到全身。成人血红蛋白包含四个蛋白质亚基-两个-球蛋白和两个-球蛋白。球蛋白的突变会导致镰状细胞病和-地中海贫血。但是人类有另一种血红蛋白亚单位基因(γ -球蛋白),它在胎儿发育过程中代替β -球蛋白表达。γ -球蛋白与α -球蛋白结合形成HbF。通常在出生前后,γ -球蛋白的表达被关闭,而β -球蛋白被打开,导致HbF向成人血红蛋白的转换。

图2 VHL基因干扰诱导胎儿血红蛋白(HbF)
“我们多年前就知道,出生后持续表达HbF可以缓解镰状细胞病和-地中海贫血的症状,”通讯作者Mitchell J. Weiss博士说,他是圣犹大血液科主任。“非常高的HbF水平可以治愈这些疾病,尽管存在缺陷的-球蛋白基因。因此,许多实验室都专注于了解围产期从γ -球蛋白基因表达到β -球蛋白基因表达的转变,并找出用药物或基因疗法逆转这一转变的新方法。”

图3 通讯作者Mitchell J Weiss医学博士,圣犹大血液科主任医师;第一作者Ruopeng Feng,圣犹大血液科博士
恢复成人HbF的产生
圣犹大研究小组发现,缺氧诱导因子1 (HIF1)直接促进γ -球蛋白基因的转录,以增强HbF的产生。HIF1是细胞感知和适应缺氧条件能力的重要组成部分。在低氧条件下,HIF1在许多组织中聚集并激活数百个基因,包括红细胞中的HbF。
第一作者Ruopeng Feng博士是Weiss实验室的一名科学家,他证明了一种可以激活部分细胞缺氧反应的药物可以抑制来自镰状细胞病成人的红细胞的镰状化。这种药物是一种脯氨酸羟化酶抑制剂,它导致HIF1积累,结合γ-球蛋白基因附近的DNA调控区,激活其转录产生HbF,抑制细胞镰状细胞。脯氨酸羟化酶抑制剂目前正处于治疗慢性肾脏疾病相关贫血的晚期临床研发阶段。这些药物通过稳定HIF蛋白来刺激促红细胞生成素的产生,促红细胞生成素是一种促进红细胞产生的激素。
Weiss说:“我们的研究结果表明,脯氨酸羟化酶抑制剂可能对治疗镰状细胞病或乙型地中海贫血有用,在这些疾病中,启动HbF产生具有治疗效益。大约20%的成年镰状细胞病患者会出现肾衰竭和相关贫血。脯氨酸羟化酶抑制剂可能对这些人有双重作用,通过刺激促红细胞生成素和HbF的产生。”
将缺氧反应与HbF联系起来
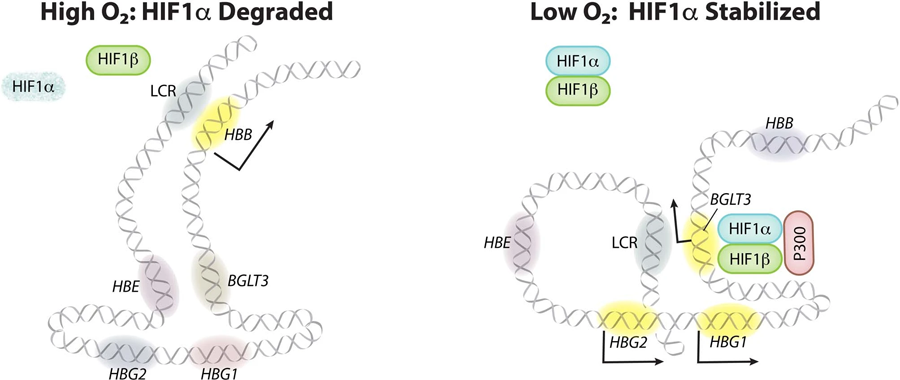
图4 成人型红细胞中HIF1α激活γ-珠蛋白转录的模型(HbF)
2019年,诺贝尔生理学或医学奖授予了HIF通路的发现。目前,由Weiss团队领导的研究建立了这种缺氧适应和HbF表达之间的直接联系。这种联系解释了长期以来的临床观察,即HbF是在暴露于缺氧或某些形式的贫血(称为“应激性红细胞生成”)后红细胞加速生成过程中诱导的。
Weiss说:“球蛋白作为HIF靶基因的鉴定支持了HbF进化为一种对抗缺氧的保护机制的概念。对血红蛋白50多年的研究确立了生物学和医学上的许多普遍原则。对血红蛋白和球蛋白基因表达的研究不断产生新的临床相关发现,这是令人兴奋和欣慰的。”
参考资料:
[1] Activation of γ-globin expression by hypoxia-inducible factor 1α
摘要:圣犹大儿童研究医院的科学家们发现,细胞对低氧的反应也会增加成人胎儿血红蛋白的表达,这可能会导致一些常见遗传性贫血的新疗法。
圣犹大儿童研究医院(St. Jude Children’s Research Hospital)的科学家已经展示了一种负责适应低氧环境(缺氧)的蛋白质是如何导致成人胎儿血红蛋白(HbF)表达增加的。这一发现对治疗镰状细胞病和乙型地中海贫血有一定的意义,这两种严重的血液疾病影响着数百万人。这项研究发表在今天的《Nature》。

图1 研究发现适应低氧环境的蛋白质是如何导致成人胎儿血红蛋白(HbF)表达增加(图源:[1])
血红蛋白就像一块蛋白质海绵,它能吸收氧气,并允许红血球将氧气运送到全身。成人血红蛋白包含四个蛋白质亚基-两个-球蛋白和两个-球蛋白。球蛋白的突变会导致镰状细胞病和-地中海贫血。但是人类有另一种血红蛋白亚单位基因(γ -球蛋白),它在胎儿发育过程中代替β -球蛋白表达。γ -球蛋白与α -球蛋白结合形成HbF。通常在出生前后,γ -球蛋白的表达被关闭,而β -球蛋白被打开,导致HbF向成人血红蛋白的转换。

图2 VHL基因干扰诱导胎儿血红蛋白(HbF)
“我们多年前就知道,出生后持续表达HbF可以缓解镰状细胞病和-地中海贫血的症状,”通讯作者Mitchell J. Weiss博士说,他是圣犹大血液科主任。“非常高的HbF水平可以治愈这些疾病,尽管存在缺陷的-球蛋白基因。因此,许多实验室都专注于了解围产期从γ -球蛋白基因表达到β -球蛋白基因表达的转变,并找出用药物或基因疗法逆转这一转变的新方法。”

图3 通讯作者Mitchell J Weiss医学博士,圣犹大血液科主任医师;第一作者Ruopeng Feng,圣犹大血液科博士
恢复成人HbF的产生
圣犹大研究小组发现,缺氧诱导因子1 (HIF1)直接促进γ -球蛋白基因的转录,以增强HbF的产生。HIF1是细胞感知和适应缺氧条件能力的重要组成部分。在低氧条件下,HIF1在许多组织中聚集并激活数百个基因,包括红细胞中的HbF。
第一作者Ruopeng Feng博士是Weiss实验室的一名科学家,他证明了一种可以激活部分细胞缺氧反应的药物可以抑制来自镰状细胞病成人的红细胞的镰状化。这种药物是一种脯氨酸羟化酶抑制剂,它导致HIF1积累,结合γ-球蛋白基因附近的DNA调控区,激活其转录产生HbF,抑制细胞镰状细胞。脯氨酸羟化酶抑制剂目前正处于治疗慢性肾脏疾病相关贫血的晚期临床研发阶段。这些药物通过稳定HIF蛋白来刺激促红细胞生成素的产生,促红细胞生成素是一种促进红细胞产生的激素。
Weiss说:“我们的研究结果表明,脯氨酸羟化酶抑制剂可能对治疗镰状细胞病或乙型地中海贫血有用,在这些疾病中,启动HbF产生具有治疗效益。大约20%的成年镰状细胞病患者会出现肾衰竭和相关贫血。脯氨酸羟化酶抑制剂可能对这些人有双重作用,通过刺激促红细胞生成素和HbF的产生。”
将缺氧反应与HbF联系起来

图4 成人型红细胞中HIF1α激活γ-珠蛋白转录的模型(HbF)
2019年,诺贝尔生理学或医学奖授予了HIF通路的发现。目前,由Weiss团队领导的研究建立了这种缺氧适应和HbF表达之间的直接联系。这种联系解释了长期以来的临床观察,即HbF是在暴露于缺氧或某些形式的贫血(称为“应激性红细胞生成”)后红细胞加速生成过程中诱导的。
Weiss说:“球蛋白作为HIF靶基因的鉴定支持了HbF进化为一种对抗缺氧的保护机制的概念。对血红蛋白50多年的研究确立了生物学和医学上的许多普遍原则。对血红蛋白和球蛋白基因表达的研究不断产生新的临床相关发现,这是令人兴奋和欣慰的。”
参考资料:
[1] Activation of γ-globin expression by hypoxia-inducible factor 1α



