摘要:麻省总医院领导的研究团队近日报告称,一种新的CRISPR-Cas9变体不需要PAM序列,就能在体外对任何DNA碱基进行切割。
麻省总医院领导的研究团队近日报告称,一种新的CRISPR-Cas9变体不需要PAM序列,就能在体外对任何DNA碱基进行切割。这种可在几乎任意位点实现精确切割的能力有望应用在多个DNA工程领域。

图1 新的CRISPR-Cas9变体能在体外对任何DNA碱基进行切割(图源:[1])
通常来说,野生型CRISPR-Cas9或Cas12酶需要先识别PAM序列,才能与靶位点结合。同样,限制性内切酶也只能在特定的DNA位点上进行切割。
麻省总医院的助理研究员Benjamin Kleinstiver表示:“对于体外应用而言,这意味着研究人员没有足够的灵活性来切割任意位点上的DNA,因为我们使用的工具正受到这些短的序列motif的限制。”
于是,麻省总医院的研究人员在2020年设计出一种近乎不受PAM限制的变体,并将其命名为SpRY。近日,Kleinstiver及其同事在《Nature Biotechnology》杂志上报告称,SpRY DNA消化(SpRYgest)过程可在体外切割几乎任何DNA序列。他们进一步优化了消化过程(包括向导RNA合成),以便其能够更广泛地应用。
在分析过程中,研究人员首先比较了野生型SpCas9和变体SpRY在20个不同位点上产生双链断裂的能力。在20个向导RNA(gRNA)的帮助下,SpCas9可消化其中的4个位点,而SpRY可消化其中的19个位点。
之后,他们比较了野生型SpCas9以及变体SpRY和SpG在64个位点上的活性,SpG也是一种变体,可识别特定的PAM序列。他们的结果突出了SpCas9对NGG PAM的偏好以及SpG对NGN PAM的偏好。相反,SpRY可近乎完全消化64个位点中的59个,表明它确实几乎不受PAM序列的限制。
SpRYgest可以用在一系列应用中。例如,它可与等温组装方法一起用在分子克隆中,比如质粒交换。此外,正如研究人员在论文中所指出的,SpRYgest可用来生成饱和突变文库,去除NGS文库中不想要的序列,以及测序方案中的靶向富集。
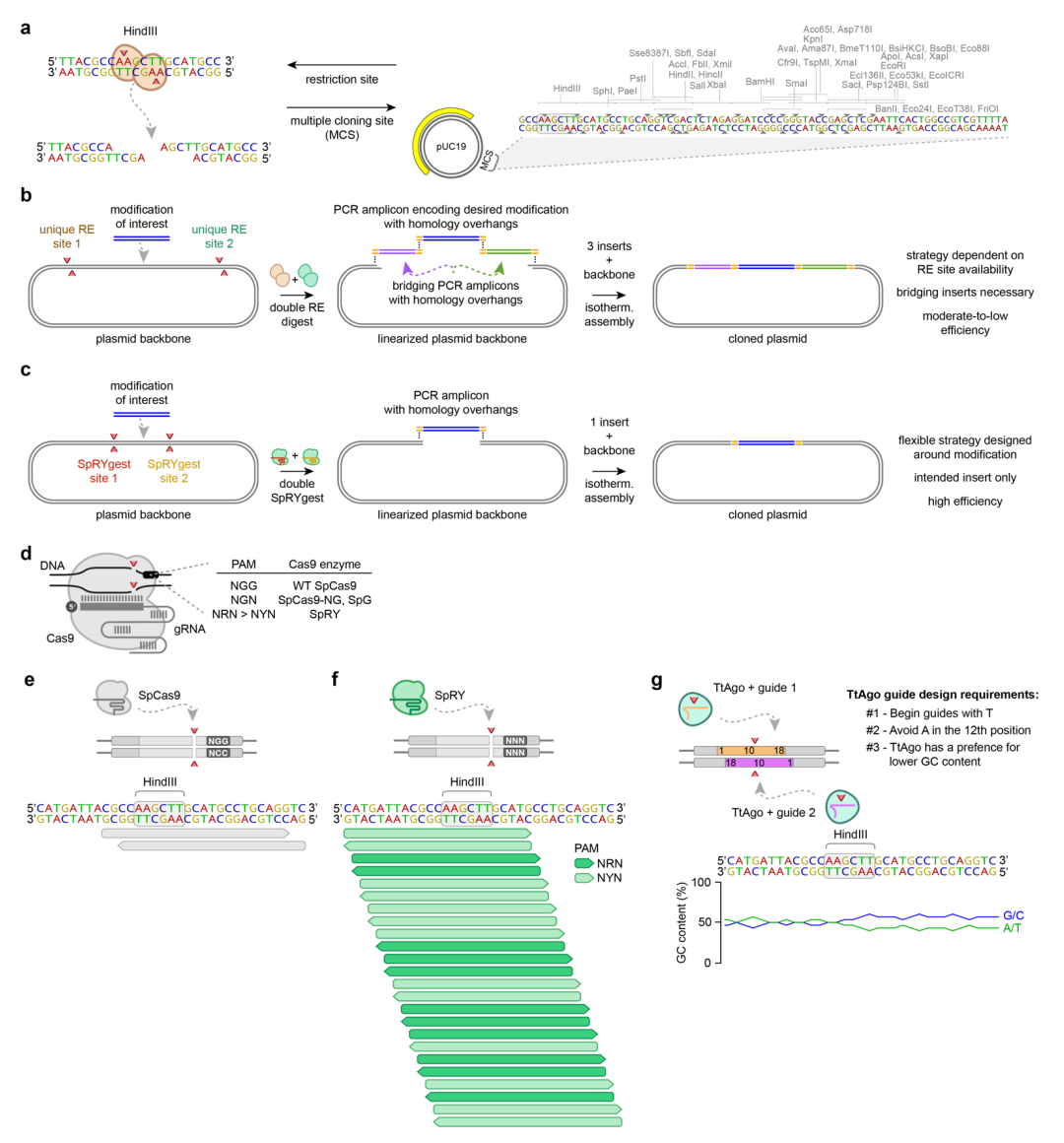
图2 DNA靶向核酸内切酶的比较(图源:[1])
为了让SpRYgest得到更广泛的应用,研究人员还对gRNA合成方案进行了改进。他们将模板生成与体外转录(IVT)步骤相结合,将IVT反应时间缩短至4小时以内。研究人员指出,这种one-pot的gRNA合成方法缩短了手动操作时间,降低了实验成本,让SpRYgest流程更类似于其他分子克隆方法。
Kleinstiver指出,这些优化方案让SpRYgest更容易实施。“寡核苷酸可以从供应商处购买,gRNA转录试剂盒也可以买到,我们希望以后还可以买到SpRY酶,”他说。他们希望用户能够将SpRYgest方法融入现有的分子克隆流程中。
参考资料:
[1] Christie, K.A., Guo, J.A., Silverstein, R.A. et al. Precise DNA cleavage using CRISPR-SpRYgests. Nat Biotechnol (2022). https://doi.org/10.1038/s41587-022-01492-y
摘要:麻省总医院领导的研究团队近日报告称,一种新的CRISPR-Cas9变体不需要PAM序列,就能在体外对任何DNA碱基进行切割。
麻省总医院领导的研究团队近日报告称,一种新的CRISPR-Cas9变体不需要PAM序列,就能在体外对任何DNA碱基进行切割。这种可在几乎任意位点实现精确切割的能力有望应用在多个DNA工程领域。

图1 新的CRISPR-Cas9变体能在体外对任何DNA碱基进行切割(图源:[1])
通常来说,野生型CRISPR-Cas9或Cas12酶需要先识别PAM序列,才能与靶位点结合。同样,限制性内切酶也只能在特定的DNA位点上进行切割。
麻省总医院的助理研究员Benjamin Kleinstiver表示:“对于体外应用而言,这意味着研究人员没有足够的灵活性来切割任意位点上的DNA,因为我们使用的工具正受到这些短的序列motif的限制。”
于是,麻省总医院的研究人员在2020年设计出一种近乎不受PAM限制的变体,并将其命名为SpRY。近日,Kleinstiver及其同事在《Nature Biotechnology》杂志上报告称,SpRY DNA消化(SpRYgest)过程可在体外切割几乎任何DNA序列。他们进一步优化了消化过程(包括向导RNA合成),以便其能够更广泛地应用。
在分析过程中,研究人员首先比较了野生型SpCas9和变体SpRY在20个不同位点上产生双链断裂的能力。在20个向导RNA(gRNA)的帮助下,SpCas9可消化其中的4个位点,而SpRY可消化其中的19个位点。
之后,他们比较了野生型SpCas9以及变体SpRY和SpG在64个位点上的活性,SpG也是一种变体,可识别特定的PAM序列。他们的结果突出了SpCas9对NGG PAM的偏好以及SpG对NGN PAM的偏好。相反,SpRY可近乎完全消化64个位点中的59个,表明它确实几乎不受PAM序列的限制。
SpRYgest可以用在一系列应用中。例如,它可与等温组装方法一起用在分子克隆中,比如质粒交换。此外,正如研究人员在论文中所指出的,SpRYgest可用来生成饱和突变文库,去除NGS文库中不想要的序列,以及测序方案中的靶向富集。

图2 DNA靶向核酸内切酶的比较(图源:[1])
为了让SpRYgest得到更广泛的应用,研究人员还对gRNA合成方案进行了改进。他们将模板生成与体外转录(IVT)步骤相结合,将IVT反应时间缩短至4小时以内。研究人员指出,这种one-pot的gRNA合成方法缩短了手动操作时间,降低了实验成本,让SpRYgest流程更类似于其他分子克隆方法。
Kleinstiver指出,这些优化方案让SpRYgest更容易实施。“寡核苷酸可以从供应商处购买,gRNA转录试剂盒也可以买到,我们希望以后还可以买到SpRY酶,”他说。他们希望用户能够将SpRYgest方法融入现有的分子克隆流程中。
参考资料:
[1] Christie, K.A., Guo, J.A., Silverstein, R.A. et al. Precise DNA cleavage using CRISPR-SpRYgests. Nat Biotechnol (2022). https://doi.org/10.1038/s41587-022-01492-y



