摘要:研究人员揭示了包括SARS-CoV-2、SARS-CoV-1和MERS-CoV在内的冠状病毒如何利用一种称为“半胱氨酸天冬氨酸蛋白酶6”(Caspase-6)的宿主蛋白酶进行有效复制的机制。
冠状病毒的核糖核酸(RNA)进入宿主细胞后,会触发感染细胞分泌干扰素,抑制病毒在感染细胞内复制,降低其他未感染细胞之间的感染风险。同时,宿主细胞也会发生凋亡过程,即程序化的细胞死亡过程,使细胞不再成为病毒复制的工厂。因此,干扰素反应和细胞凋亡是人类和动物细胞中很重要的抗病毒机制。
细胞凋亡是由半胱氨酸-天冬氨酸蛋白酶在人和动物细胞中执行的,通过该蛋白酶清除感染细胞以抑制病毒复制。香港大学医学院的研究小组研究了caspase-6在一系列细胞系、人离体肺组织、人肠道类器官和动物模型中对冠状病毒复制的影响。研究小组发现,caspase-6的化学抑制或基因缺失显著降低了冠状病毒的复制,而过表达caspase-6有效地促进了冠状病毒的复制。
图1 caspase-6在一系列细胞系、人离体肺组织、人肠道类器官和动物模型中对冠状病毒复制的影响(图源:[1])
研究方法和结果
在小鼠模型中,caspase-6的化学抑制剂极大地限制了小鼠适应的MERS-CoV (MERS-CoVMA)的复制,并显著地将小鼠的存活率从33.3%提高到80%。此外,在caspase-6敲除小鼠的肺中,MERS-CoVMA复制和MERS-CoVMA诱导的肺损伤明显减少。同样,在仓鼠模型中,针对caspase-6的特异性化学抑制剂减少了SARS-CoV-2的复制和相关的炎症性肺损伤。
但冠状病毒如何利用caspase-6来造福自己呢?请注意,干扰素反应是宿主细胞重要和直接的抗病毒防御。我们的进一步研究发现,caspase-6可以切割冠状病毒核衣壳(N)蛋白,产生N个片段,与宿主的“干扰素调控因子3 (IRF3)”相互作用,阻止其进入细胞核启动干扰素应答。因此,病毒N片段作为干扰素拮抗剂,促进病毒复制。
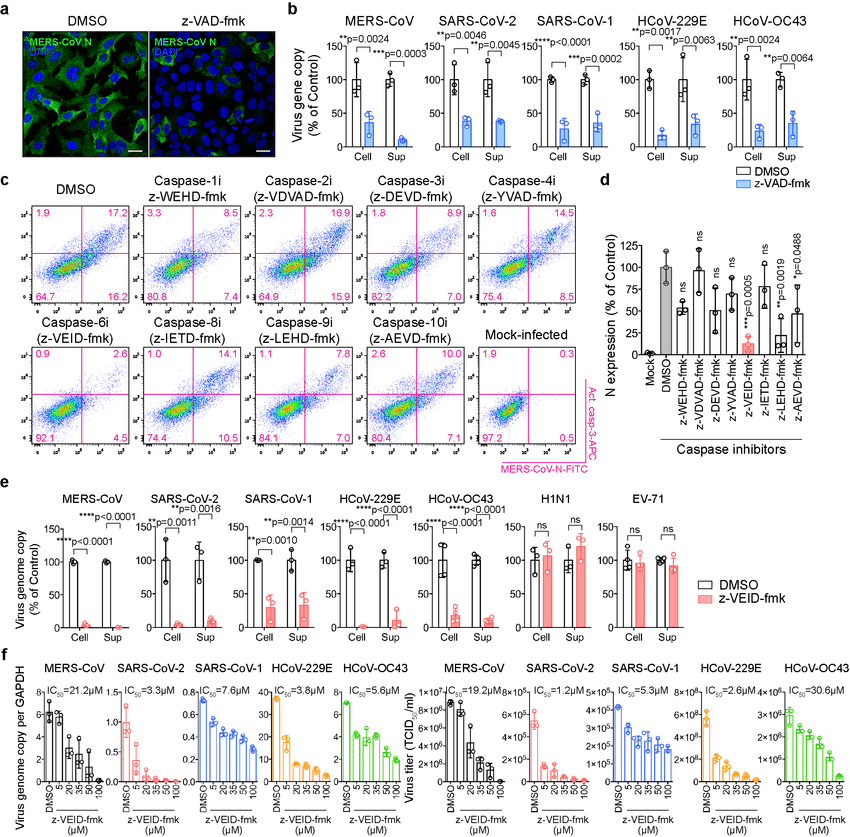
图2 在小鼠模型中,caspase-6的化学抑制剂极大地限制了小鼠适应的MERS-CoV (MERS-CoVMA)的复制(图源:[1])
研究意义
这项研究显示了冠状病毒是如何进化成很成功的病原体的。我们揭示了冠状病毒如何克服宿主细胞对干扰素反应的抗病毒防御的一种新机制,通过开发一类新的宿主蛋白酶,caspase-6,该蛋白酶原本是宿主用来执行细胞凋亡,作为一种防御病毒感染,以获得更好的病毒复制。这些结果进一步表明,可以设计针对caspase-6的药物,它可以成为所有已知人类冠状病毒感染抗病毒治疗的潜在干预目标。
参考资料:
[1] Hin Chu, Yuxin Hou, Dong Yang, Lei Wen, Huiping Shuai, Chaemin Yoon, Jialu Shi, Yue Chai, Terrence Tsz-Tai Yuen, Bingjie Hu, Cun Li, Xiaoyu Zhao, Yixin Wang, Xiner Huang, Kin Shing Lee, Luo Cuiting, Jian-Piao Cai, Vincent Kwok-Man Poon, Chris Chung-Sing Chan, Anna Jinxia Zhang, Shuofeng Yuan, Ko-Yung Sit, Dominic Chi-Chung Foo, Wing-Kuk Au, Kenneth Kak-Yuen Wong, Jie Zhou, Kin-Hang Kok, Dong-Yan Jin, Jasper Fuk-Woo Chan, Kwok-Yung Yuen. Coronaviruses exploit a host cysteine-aspartic protease for replication. Nature, 2022
摘要:研究人员揭示了包括SARS-CoV-2、SARS-CoV-1和MERS-CoV在内的冠状病毒如何利用一种称为“半胱氨酸天冬氨酸蛋白酶6”(Caspase-6)的宿主蛋白酶进行有效复制的机制。
冠状病毒的核糖核酸(RNA)进入宿主细胞后,会触发感染细胞分泌干扰素,抑制病毒在感染细胞内复制,降低其他未感染细胞之间的感染风险。同时,宿主细胞也会发生凋亡过程,即程序化的细胞死亡过程,使细胞不再成为病毒复制的工厂。因此,干扰素反应和细胞凋亡是人类和动物细胞中重要的抗病毒机制。
细胞凋亡是由半胱氨酸-天冬氨酸蛋白酶在人和动物细胞中执行的,通过该蛋白酶清除感染细胞以抑制病毒复制。香港大学医学院的研究小组研究了caspase-6在一系列细胞系、人离体肺组织、人肠道类器官和动物模型中对冠状病毒复制的影响。研究小组发现,caspase-6的化学抑制或基因缺失显著降低了冠状病毒的复制,而过表达caspase-6有效地促进了冠状病毒的复制。

图1 caspase-6在一系列细胞系、人离体肺组织、人肠道类器官和动物模型中对冠状病毒复制的影响(图源:[1])
研究方法和结果
在小鼠模型中,caspase-6的化学抑制剂极大地限制了小鼠适应的MERS-CoV (MERS-CoVMA)的复制,并显著地将小鼠的存活率从33.3%提高到80%。此外,在caspase-6敲除小鼠的肺中,MERS-CoVMA复制和MERS-CoVMA诱导的肺损伤明显减少。同样,在仓鼠模型中,针对caspase-6的特异性化学抑制剂减少了SARS-CoV-2的复制和相关的炎症性肺损伤。
但冠状病毒如何利用caspase-6来造福自己呢?请注意,干扰素反应是宿主细胞重要和直接的抗病毒防御。我们的进一步研究发现,caspase-6可以切割冠状病毒核衣壳(N)蛋白,产生N个片段,与宿主的“干扰素调控因子3 (IRF3)”相互作用,阻止其进入细胞核启动干扰素应答。因此,病毒N片段作为干扰素拮抗剂,促进病毒复制。

图2 在小鼠模型中,caspase-6的化学抑制剂极大地限制了小鼠适应的MERS-CoV (MERS-CoVMA)的复制(图源:[1])
研究意义
这项研究显示了冠状病毒是如何进化成很成功的病原体的。我们揭示了冠状病毒如何克服宿主细胞对干扰素反应的抗病毒防御的一种新机制,通过开发一类新的宿主蛋白酶,caspase-6,该蛋白酶原本是宿主用来执行细胞凋亡,作为一种防御病毒感染,以获得更好的病毒复制。这些结果进一步表明,可以设计针对caspase-6的药物,它可以成为所有已知人类冠状病毒感染抗病毒治疗的潜在干预目标。
参考资料:
[1] Hin Chu, Yuxin Hou, Dong Yang, Lei Wen, Huiping Shuai, Chaemin Yoon, Jialu Shi, Yue Chai, Terrence Tsz-Tai Yuen, Bingjie Hu, Cun Li, Xiaoyu Zhao, Yixin Wang, Xiner Huang, Kin Shing Lee, Luo Cuiting, Jian-Piao Cai, Vincent Kwok-Man Poon, Chris Chung-Sing Chan, Anna Jinxia Zhang, Shuofeng Yuan, Ko-Yung Sit, Dominic Chi-Chung Foo, Wing-Kuk Au, Kenneth Kak-Yuen Wong, Jie Zhou, Kin-Hang Kok, Dong-Yan Jin, Jasper Fuk-Woo Chan, Kwok-Yung Yuen. Coronaviruses exploit a host cysteine-aspartic protease for replication. Nature, 2022



