入侵的军队需要稳定的燃料和武器供应。当入侵者是细胞时也是如此,比如当肿瘤细胞从它们的邻居中分离出来,并在一种被称为转移的过程中扩散到身体的其他部位时——这是癌症致命的部分。
现在,杜克大学领导的一项关于微小蠕虫秀丽隐杆线虫的研究,为入侵细胞如何积聚和部署燃料到入侵前线提供了新的见解,为它们的细胞突破机制提供动力。
在发表在《发育细胞》杂志上的一项研究中,杜克大学生物学教授大卫·舍伍德和他的同事们发现了两种葡萄糖转运体,当它们失去活性时,会破坏入侵蠕虫细胞的能量供应,甚至会阻止一些蠕虫细胞前进。
这一发现可能导致新的方法来切断癌细胞在人类体内转移的供应线。
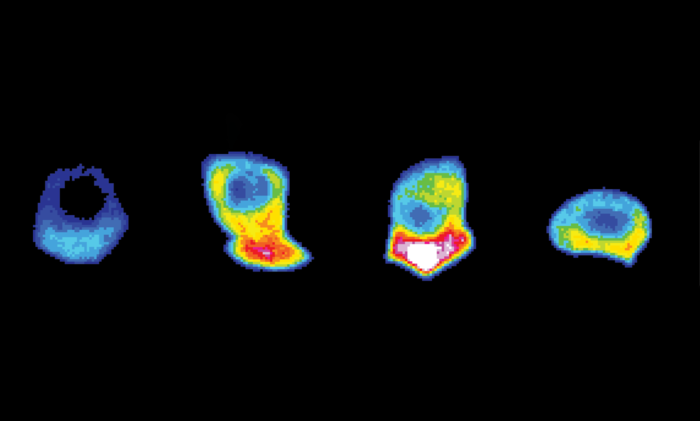
图片:这是一个比一粒沙子小数百倍的小虫细胞的延时拍摄,显示了细胞内ATP能量的水平,在它侵入其他组织之前,期间和之后。
图片来源:杜克大学Aastha Garde
舍伍德说:“这是一件大事,因为它为我们提供了侵入性细胞治疗的一个新方面。”
众所周知,转移性癌症很难治疗。大多数抗癌药物通过破坏肿瘤细胞或减缓其生长来发挥作用。但是,在200多种已被批准用于临床使用的抗癌药物中,很少有药物能够真正防止癌症从原始肿瘤分裂并扩散到其他器官——而这正是绝大多数癌症相关死亡的罪魁祸首。
“我们没有针对这一步的治疗方法,因为我们对细胞如何突破组织屏障还没有很好的了解,”该论文的作者舍伍德说。“这很讽刺,因为这是癌症致命的一面,但也是我们不了解的一面。”
部分原因是这个过程很难研究。癌症的扩散是不可预测的,大多数癌细胞转移到身体深处,在光学显微镜观察不到的地方。
舍伍德说:“很难在行为中发现入侵细胞。”
因此,舍伍德的实验室对一种名为秀丽隐杆线虫的毫米长的透明蠕虫进行了类似的研究。在发育中的蠕虫完成其生殖道的构建之前,一种被称为锚细胞的特殊细胞必须打破将蠕虫的子宫和外阴分开的致密的薄片状网状结构,为交配和产卵扫清道路。
蠕虫细胞和人类癌细胞都使用同样的侵入机制:从细胞表面冒出一连串活塞状的突起,猛击组织屏障,为细胞清理出一条通路,就像冲出一条逃生通道一样。
问题是,“这些机器的燃料是什么?”杜克大学细胞生物学博士生、作者Aastha Garde说。“我们能不能以它为目标,而不是以机器本身为目标,剥夺它们的能源,让机器停止工作?”
研究人员使用一架连接在高倍显微镜上的摄像机,观察比一粒沙子小数百倍的微小蠕虫细胞内部,并观察它们“闯入”的行动。
加德展示了一个入侵细胞的延时拍摄,当它推进并楔入邻近的组织。这种细胞被设计了一个传感器,当一种叫做ATP的携带能量的分子达到一定水平时,它就会发光,就像细胞燃料计一样。就在细胞即将突破的时候,细胞前线后面出现了一束光,显示出在突破时大量的ATP。
研究人员表示,这种ATP是由一种叫做线粒体的细胞器产生的,线粒体是细胞的能量工厂,它被一种叫做netrin的分子线索引导到细胞的入侵前线。
研究人员还筛选了蛔虫大约2万个基因中的8300个,用一种叫做RNA干扰的技术逐个沉默它们,看看蛔虫细胞是否仍然能够突破。
他们发现了两种编码门状蛋白质的基因,分别是FGT-1和FGT-2。这些细胞在入侵前沿着细胞的边缘堆积起来,让更多的葡萄糖进入细胞,在那里葡萄糖被分解成ATP。
当研究人员使这些基因失活时,葡萄糖和ATP水平下降,蠕虫细胞停止了它们的传播。通过显微镜,他们可以看到细胞在微弱地伸出新的活塞状突起,想要通过,但大多数细胞都被推迟了,三分之一的细胞停止了前进。
加德说:“如果没有葡萄糖,锚定细胞穿透基底膜的整个机制基本上都会受损。”
关于癌细胞转移的原因,还有很多科学家还不清楚。但舍伍德说,研究人员希望他们对蠕虫的研究能帮助他们“找到细胞入侵的致命弱点”。
舍伍德说:“这是细胞如何破坏的一个方面,在很大程度上被忽视了。”“如果我们能阻止ATP的爆发,我们就能限制或阻止细胞入侵。”
文章标题
Localized Glucose Import, Glycolytic Processing, and Mitochondria Generate a Focused ATP Burst to Power Basement Membrane Invasion
入侵的军队需要稳定的燃料和武器供应。当入侵者是细胞时也是如此,比如当肿瘤细胞从它们的邻居中分离出来,并在一种被称为转移的过程中扩散到身体的其他部位时——这是癌症致命的部分。
现在,杜克大学领导的一项关于微小蠕虫秀丽隐杆线虫的研究,为入侵细胞如何积聚和部署燃料到入侵前线提供了新的见解,为它们的细胞突破机制提供动力。
在发表在《发育细胞》杂志上的一项研究中,杜克大学生物学教授大卫·舍伍德和他的同事们发现了两种葡萄糖转运体,当它们失去活性时,会破坏入侵蠕虫细胞的能量供应,甚至会阻止一些蠕虫细胞前进。
这一发现可能导致新的方法来切断癌细胞在人类体内转移的供应线。

图片:这是一个比一粒沙子小数百倍的小虫细胞的延时拍摄,显示了细胞内ATP能量的水平,在它侵入其他组织之前,期间和之后。
图片来源:杜克大学Aastha Garde
舍伍德说:“这是一件大事,因为它为我们提供了侵入性细胞治疗的一个新方面。”
众所周知,转移性癌症很难治疗。大多数抗癌药物通过破坏肿瘤细胞或减缓其生长来发挥作用。但是,在200多种已被批准用于临床使用的抗癌药物中,很少有药物能够真正防止癌症从原始肿瘤分裂并扩散到其他器官——而这正是绝大多数癌症相关死亡的罪魁祸首。
“我们没有针对这一步的治疗方法,因为我们对细胞如何突破组织屏障还没有很好的了解,”该论文的作者舍伍德说。“这很讽刺,因为这是癌症致命的一面,但也是我们不了解的一面。”
部分原因是这个过程很难研究。癌症的扩散是不可预测的,大多数癌细胞转移到身体深处,在光学显微镜观察不到的地方。
舍伍德说:“很难在行为中发现入侵细胞。”
因此,舍伍德的实验室对一种名为秀丽隐杆线虫的毫米长的透明蠕虫进行了类似的研究。在发育中的蠕虫完成其生殖道的构建之前,一种被称为锚细胞的特殊细胞必须打破将蠕虫的子宫和外阴分开的致密的薄片状网状结构,为交配和产卵扫清道路。
蠕虫细胞和人类癌细胞都使用同样的侵入机制:从细胞表面冒出一连串活塞状的突起,猛击组织屏障,为细胞清理出一条通路,就像冲出一条逃生通道一样。
问题是,“这些机器的燃料是什么?”杜克大学细胞生物学博士生、作者Aastha Garde说。“我们能不能以它为目标,而不是以机器本身为目标,剥夺它们的能源,让机器停止工作?”
研究人员使用一架连接在高倍显微镜上的摄像机,观察比一粒沙子小数百倍的微小蠕虫细胞内部,并观察它们“闯入”的行动。
加德展示了一个入侵细胞的延时拍摄,当它推进并楔入邻近的组织。这种细胞被设计了一个传感器,当一种叫做ATP的携带能量的分子达到一定水平时,它就会发光,就像细胞燃料计一样。就在细胞即将突破的时候,细胞前线后面出现了一束光,显示出在突破时大量的ATP。
研究人员表示,这种ATP是由一种叫做线粒体的细胞器产生的,线粒体是细胞的能量工厂,它被一种叫做netrin的分子线索引导到细胞的入侵前线。
研究人员还筛选了蛔虫大约2万个基因中的8300个,用一种叫做RNA干扰的技术逐个沉默它们,看看蛔虫细胞是否仍然能够突破。
他们发现了两种编码门状蛋白质的基因,分别是FGT-1和FGT-2。这些细胞在入侵前沿着细胞的边缘堆积起来,让更多的葡萄糖进入细胞,在那里葡萄糖被分解成ATP。
当研究人员使这些基因失活时,葡萄糖和ATP水平下降,蠕虫细胞停止了它们的传播。通过显微镜,他们可以看到细胞在微弱地伸出新的活塞状突起,想要通过,但大多数细胞都被推迟了,三分之一的细胞停止了前进。
加德说:“如果没有葡萄糖,锚定细胞穿透基底膜的整个机制基本上都会受损。”
关于癌细胞转移的原因,还有很多科学家还不清楚。但舍伍德说,研究人员希望他们对蠕虫的研究能帮助他们“找到细胞入侵的致命弱点”。
舍伍德说:“这是细胞如何破坏的一个方面,在很大程度上被忽视了。”“如果我们能阻止ATP的爆发,我们就能限制或阻止细胞入侵。”
文章标题
Localized Glucose Import, Glycolytic Processing, and Mitochondria Generate a Focused ATP Burst to Power Basement Membrane Invasion



