阿尔茨海默征作为老年前期和老年的中枢神经退行性病变,逐渐被大众熟知。目前我国大约有600万-800万名阿尔茨海默症并患者,在65岁以上的老年人群中的患病率约为3%-7%。但至今其发病原因尚不明确。
在成人大脑中,存在于海马神经源生态位的神经干细胞维持着终生的神经产生功能。成年海马神经发生(AHN)在功能上与人类和啮齿动物的记忆和认知可塑性相关。在阿尔茨海默病中,海马神经源性生态位产生新神经元的过程受到阻碍,但其机制尚不清楚。
2021年5月24日,荷兰神经科学研究所Evgenia Salta、比利时鲁汶大学Bart De Strooper等研究人员合作在国际学术期刊《细胞 - 干细胞》上在线发表了题为“Restoring miR-132 expression rescues adult hippocampal neurogenesis and memory deficits in Alzheimer's disease"的文章,文章表明:恢复miR-132的表达可挽救成年海马神经发生和阿尔茨海默氏病的记忆缺陷。

恢复miR-132的表达可挽救成年海马神经发生和阿尔茨海默氏病的记忆缺陷
首先,研究人员在10名非痴呆对照个体和10名阿尔茨海默病患者的组织切片中对海马体齿状回颗粒下区增殖的神经元祖细胞进行了死后免疫组织化学分析,证实在AD中成人神经发生受到了病理损害,并在小鼠模型中证实AD中的大脑病理损害与成人海马神经源性生态位中的 miR-132 水平相关。
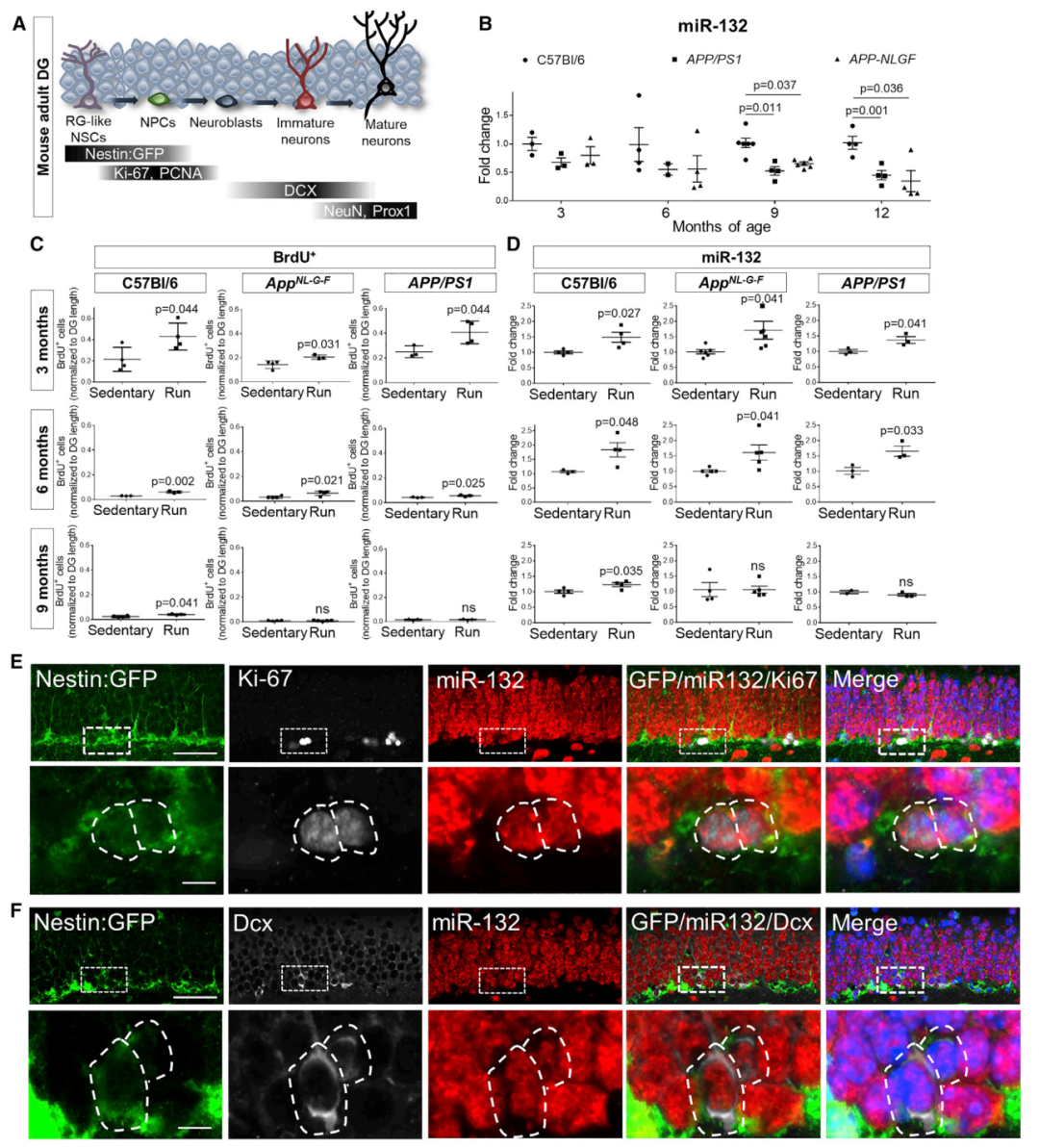
AD中成人神经发生的病理损害并与成人海马神经源性生态位中的 miR-132 水平相关
接下来,研究人员评估了miR-132在成人神经源性生态位中的定位,通过荧光分选技术证实miR-132可以被成年神经干细胞和祖细胞募集,作为对运动或衰老相关刺激反应的一部分,但在AD病理损害时在海马神经源性生态位中并未出现相同的现象。而在功能方面,实验证实miR-132是体内齿状回神经发生诱导所必需的,并且在人类神经干细胞中可以调节神经元分化而在阿尔茨海默病相关病理学中下调。

成人的神经发生需要 miR-132
后续,研究人员探究了提高miR-132水平是否能改善在阿尔茨海默病小鼠模型中观察到的AHN缺陷,实验表明miR-132可以减轻阿尔茨海默病小鼠模型脑内成体神经前体细胞的增殖和分化缺陷,并且miR-132可以通过细胞自主的方式来调节晚期神经元成熟,在成年神经干细胞和祖细胞中增加miR-132可以改善AD小鼠模型的齿状回缺陷。通过提高miR-132水平可恢复老年阿尔茨海默病小鼠的AHN相关记忆缺陷。
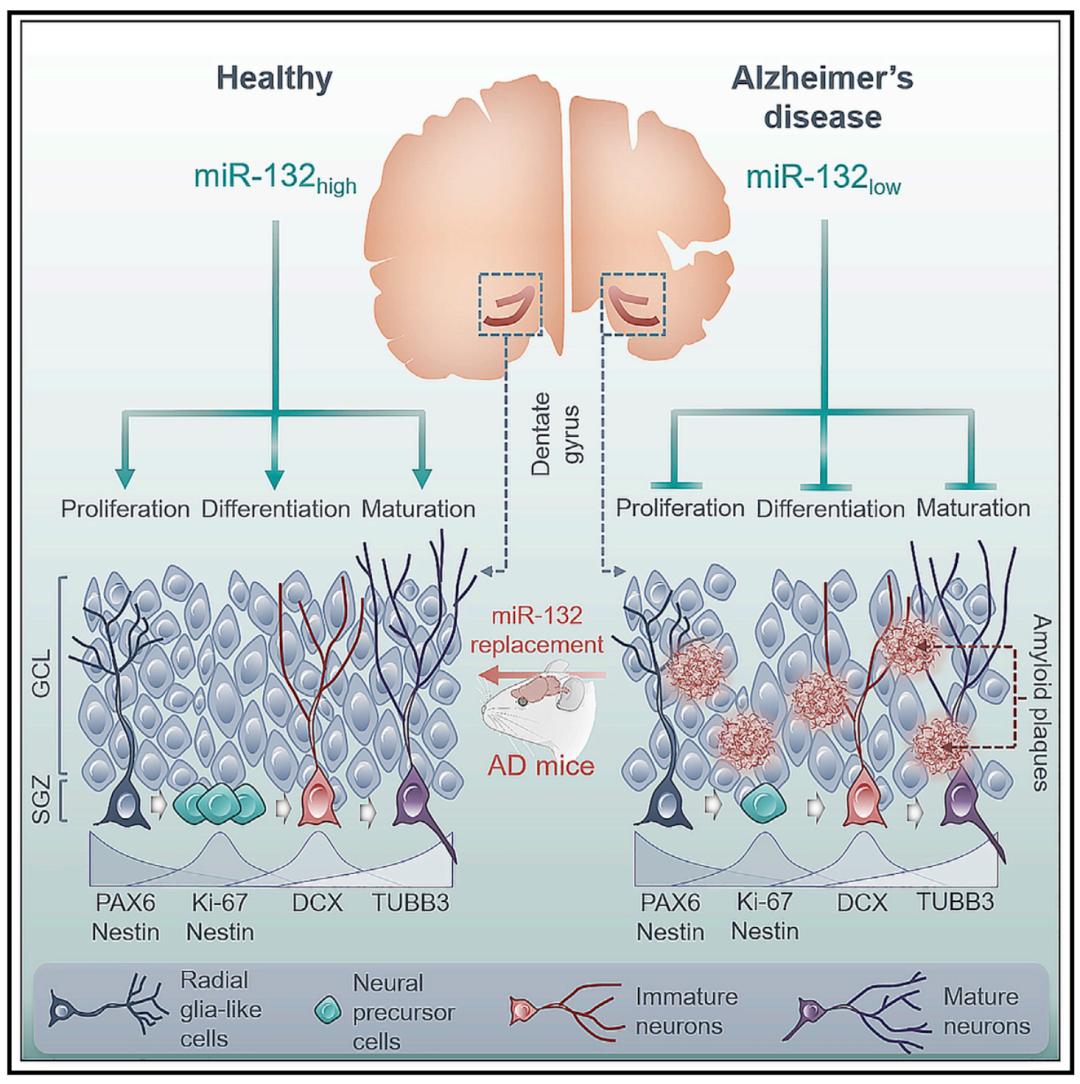
实验机制图
总之,本篇文章确定了miR-132是AD中一致下调的miRNA之一,是AHN的有效调节剂,在成人神经干细胞及其后代中发挥细胞自主前神经发生作用。使用不同的阿尔茨海默病小鼠模型、培养的人类原代和已建立的神经干细胞以及人类患者材料都证明AHN直接受阿尔茨海默病病理学影响。成年小鼠阿尔茨海默病海马中的miR-132替代物可以恢复AHN和相关的记忆缺陷。
该研究发现证实了AHN在阿尔茨海默病小鼠模型中的意义,并揭示了靶向miR-132在神经退行性变中的可能治疗潜力。



