治疗抵抗/耐药是肿瘤临床治疗面临的一个相当棘手的问题。耐药机制的发生通常涉及到细胞代谢、增殖和氧化还原状态等多种与肿瘤生存相关的信号通路,使得包括化疗、靶向治疗在内的手段大大受限。一些原本敏感的肿瘤在靶向治疗一段时间后也可能因为发生新的突变而产生耐药。因此,人们试图寻找出不同癌症靶点的共有的“弱点”并开发一种针对该“弱点”的单一治疗方法,从而克服肿瘤治疗的抵抗。
近年来,细胞活性氧类(ROS)被发现在肿瘤细胞中异常升高,并与糖酵解、氧化还原、增殖信号传导密切相关,表明其可能正是这种共有的“弱点”。此前,研究人员已经能够利用一种气体放电技术低温大气等离子体(CAP)产生外源性ROS。CAP已被FDA批准为一种导管引导手术刀,用于常规肿瘤和神经外科手术,并在头颈癌的临床试验中显示出疗效。
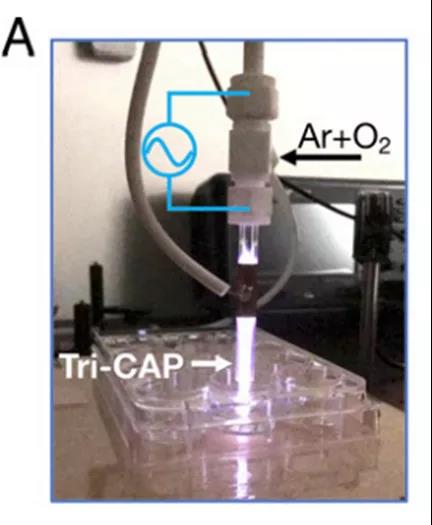
2021年,来自西安交通大学、美国欧道明大学和犹他大学的研究团队发现,在耐药的慢性髓性粒细胞白血病(CML)小鼠模型中,其开发的CAP治疗方案能够有效阻断包括氧化还原平衡失调、糖酵解和细胞增殖在内的三种癌症生存相关通路,因此将该方案命名为Trident CAP (Tri-CAP)。Tri-CAP还能造成CML和原始CD34+造血干细胞和祖细胞的高效率凋亡,同时却对非恶性的对照细胞影响甚微,其在动物实验中的良好表现也为克服白血病耐药问题带来了曙光。研究成果2021年12月21日刊登在PNAS。

现有的ROS疗法面临的主要问题是无法确定ROS的有效浓度:ROS水平太低无法诱导细胞凋亡,太高则会激活促癌的HIF-α通路。该团队很好地克服了这一难题,他们在氧气含量为3%的氩气中使用等离子体射流(速度1.9 L/min)产生ROS,电极距离细胞培养基的距离为30毫米。这种CAP方案能够在无细胞培养基中产生极低水平的ROS,远低于激活HIF-α通路所需的ROS水平,同时培养基的温度、酸碱度等其他指标则几乎未受到影响。在正常细胞、伊马替尼耐药的CML细胞(BCR-ABLT315I细胞)和伊马替尼敏感的CML细胞(BCR-ABLp210细胞)中,Tri-CAP能使耐药的细胞产生异常低水平的胞外ROS和细胞内ROS的一过性急剧升高,实现对耐药细胞系的选择性致死。
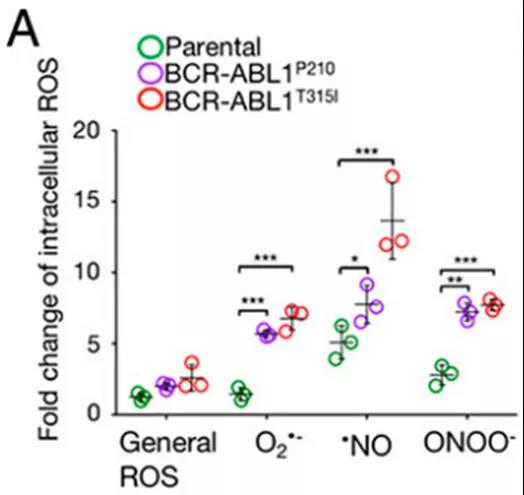
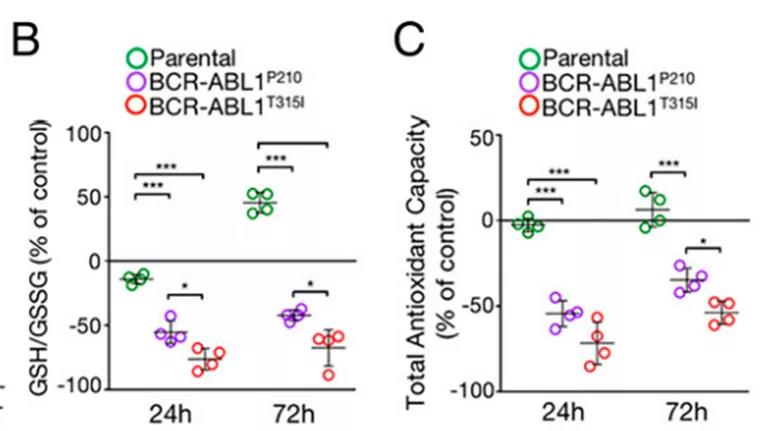
研究人员进一步发现,Tri-CAP激发的低水平ROS打破了细胞内的氧化还原平衡。在BCR-ABL1+细胞系中,Tri-CAP通过两种途径破坏氧化还原平衡:胞内过度的ROS产生和抗氧化防御减弱。相反,对照组的正常细胞在经过三次相同处理后能迅速恢复氧化还原平衡。
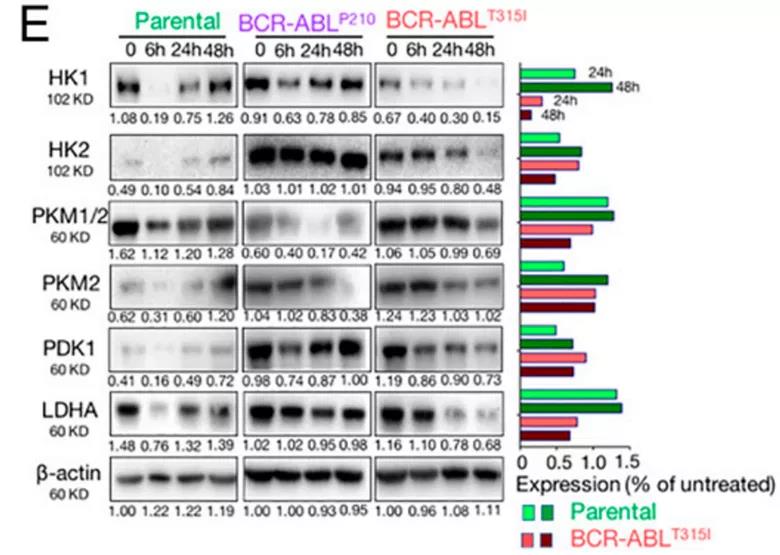
研究还发现,Tri-CAP还可以抑制肿瘤代谢过程中的多个关键靶点,并减少乳酸生产。在耐药的BCR-ABLT315I细胞中发现,有氧糖酵解中的多个关键分子如PKM2、HK1、HK2和PDK1的蛋白表达水平在Tri-CAP治疗后的0- 48小时内逐渐降低, HK1几乎缺失。
该团队进一步检测了这一疗法对该通路的影响,发现该通路激活的分子标志物如磷酸化的mTOR、磷酸化的AKT在耐药的CML细胞系中表达水平大幅下降,而在敏感的CML细胞系及对照组细胞中表达增加,促使肿瘤耐药HIF-α表达水平呈现出类似的模式。
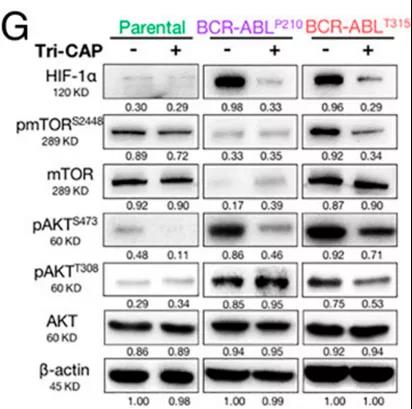
总之,这些结果表明Tri-CAP可以优先阻断抗耐药CML中氧化还原稳态、糖酵解和增殖(AKT/mTOR/HIF-1α)这三种癌症生存的关键途径,揭示了一个之前未报道过的肿瘤治疗方法。
此外,Tri-CAP还能诱导耐药细胞发生凋亡。接受Tri-CAP处理后的CML患者的CD34+造血细胞和祖细胞显示出高凋亡率。体内实验也证明这些该疗法治疗可减少肿瘤形成,提高荷瘤小鼠的存活率。
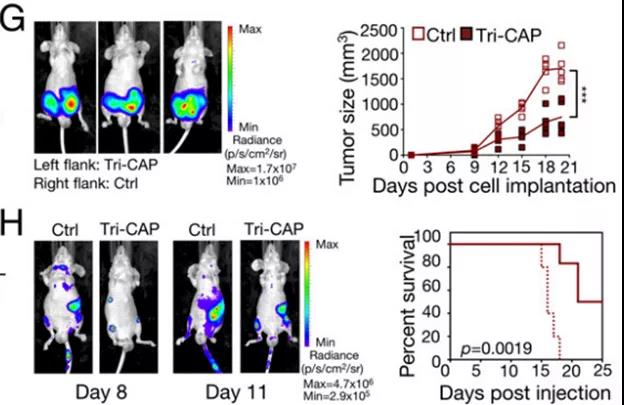
包括放疗在内的传统ROS生成治疗,通常依赖于高水平的ROS诱导癌细胞直接死亡,但同时肿瘤的生存相关通路被激活使得疗效有限。相比之下,本研究巧妙地解决了这一问题,为未来的临床研究提供了基础。总的来说,Tri-CAP有望作为一种潜在的疗法,克服和预防多种恶性肿瘤治疗耐药性。



