提到“艾滋病”三个字,相信大家都不陌生,今年12月1日是第34个“世界艾滋病日”,主题为”生命至上终结艾滋健康平等”。艾滋病也被称之为获得性免疫缺陷综合征,诱发原因是感染了HIV病毒,是当前较为严峻的公共卫生问题。
据世界卫生组织官网消息,2020年全球约有3770万艾滋病毒感染者,新感染艾滋病毒的人数为150万人,死于艾滋病毒相关原因的人数为68万人。艾滋病常与性、毒品联系紧密,目前还没有疫苗可以预防,导致人们对它极其避讳和恐惧。12月9日发表在Nature Medicine上的一篇研究进展,为开发mRNA疫苗以攻克HIV带来希望。这一研究由美国国立卫生研究院(NIH)下属过敏症和传染病研究所(NIAID)的Paolo Lusso博士领导,其他NIAID科学家、mRNA巨头Moderna和其他机构的研究人员共同合作。

研究结果显示,与未接种疫苗的对照组相比较而言,初始接种疫苗并在多次接种加强针后的恒河猴其感染猿猴-人类免疫缺陷病毒(SHIV)的概率降低了79%。并且,新型mRNA疫苗安全性较高,可以同时启动体液免疫和细胞免疫进行防疫。
新型HIV疫苗的原理与mRNA新冠疫苗类似。研究人员将编码HIV关键蛋白包膜糖蛋白Env(相当于SARS-CoV-2的S蛋白)与组特异性抗原蛋白Gag封装在脂质纳米颗粒(LNP)中,以在体内封装产生病毒样颗粒(VLP)。VLP缺乏传染性的遗传物质,但在诱发免疫反应方面与HIV相当。
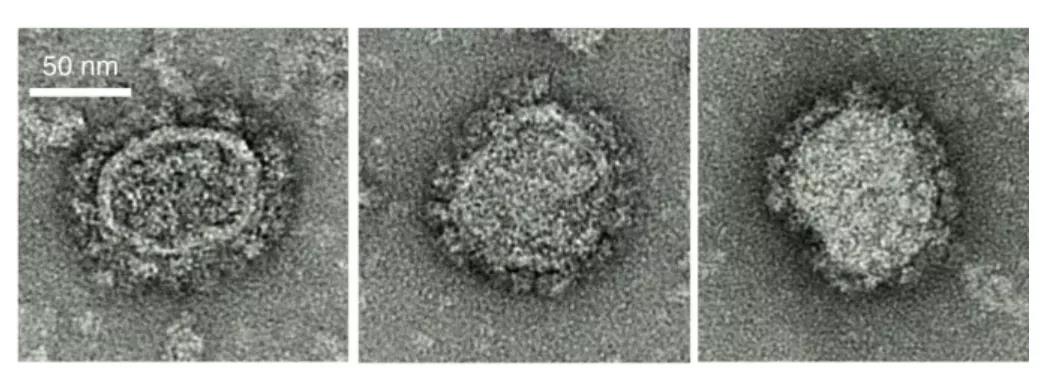
研究者在恒河猴上进行了测试,随后评估了在恒河猴中产生VLP 的env-gag mRNA疫苗的免疫原性和功效,并且用携带 HIV-1 Env 的活SHIV进行挑战。总共招募了14只幼稚雌性恒河猴(7只疫苗接种者和7只对照),接种疫苗的动物依次接受来自三个不同 HIV-1 进化枝的四env mRNA。结果表明,尽管使用高mRNA剂量进行了多次免疫,但疫苗耐受性良好,每次接种后只有轻微的不良事件。
研究者先是评估了中和抗体的引发。早在第二次自体免疫后2周(第 13 周),即可检测到低滴度的自体中和抗体,但时间非常短暂。除了第 27 周第1亚组的中和效价更高以及第37周同一亚组中V3环肽的中和作用降低更大之外,在第1和第2亚组的动物之间没有观察到自体中和的显着差异。这些结果表明蛋白质加强可能诱导了略高的 V3 特异性抗体反应。
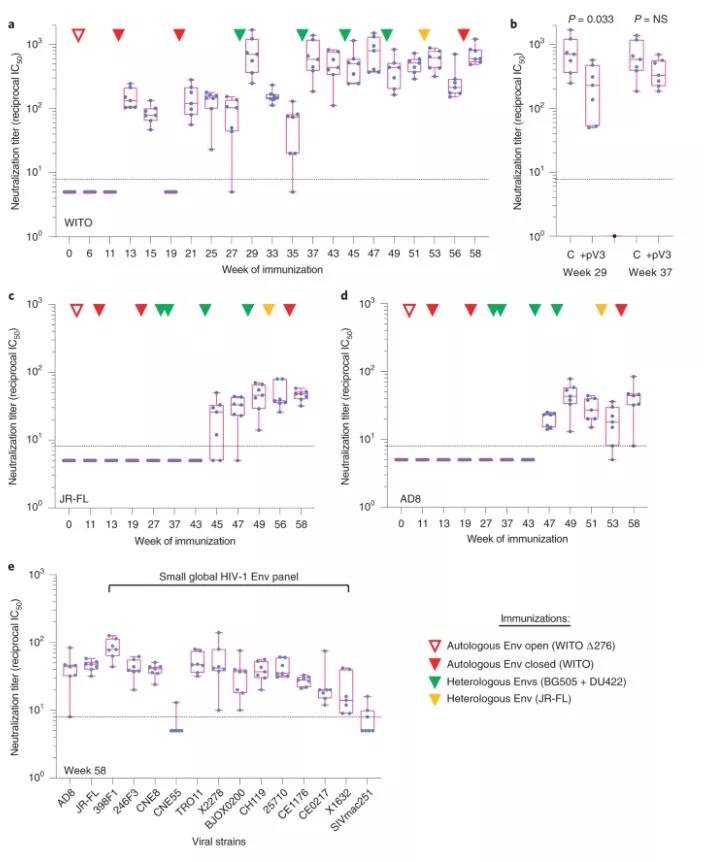
接着,在两个时间点针对疫苗表达的两种病毒抗原(即 HIV-1 Env 和 SIV Gag)测试病毒特异性T细胞反应:自体阶段完成后第27 周和第60周。在第27周时已经可检测到多功能 Env 特异性 CD4+T细胞反应,但在第60周时在所有动物中显着增强。
值得注意的是,第60周CD4+T细胞的多功能性显着增加,近50%的响应细胞共表达三种或更多细胞因子,这与引发抗体产生的强T细胞辅助活性一致。相比之下,SIV Gag 特异性CD4+和CD8+T细胞反应在第27周和第60 周都无法检测到。
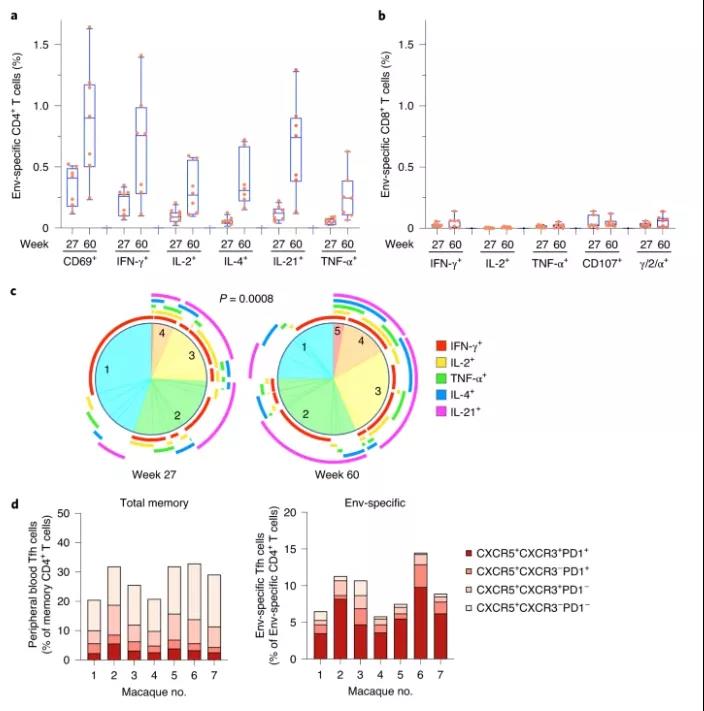
主要研究者Lusso博士表示,由mRNA翻译得到的Env与天然HIV中的Env非常类似,且实验中所用的VLP可以展示多个HIV包膜蛋白,疫苗诱发免疫反应的过程与自然感染过程非常类似。此外,mRNA还可在给药数天后继续表达,提供持续的免疫刺激。新型mRNA疫苗的另一个优势在于VLP可更好地与抗原递呈细胞结合,保证将mRNA递送到适当的细胞中,并诱导滤泡辅助T细胞以促进生发中心的形成。
总的来说,env-gag VLP mRNA平台为开发预防性HIV-1疫苗提供了一种很有前景的方法。就人类临床试验的免疫原制造所需的挑战、成本和时间而言,在给予连续数次的病毒攻击后,该疫苗仍能将每次感染的风险降低79%,因此使用mRNA作为载体可能比使用外源蛋白质免疫更具显着优势。尽管如此,该研究成果仍然需要通过大量额外的临床前和临床试验来进一步确认结果的可靠性,期待抗“艾”疫苗早日出现在大众的视野中。



