日本科学家研发出了一种抗衰老疫苗,可以诱使免疫系统选择性清除衰老细胞,延长生命。
衰老细胞广泛存在于人、灵长类动物和啮齿类动物的组织中,并且在人类的年龄相关的疾病,如骨关节炎、肺纤维化、动脉粥样硬化和阿尔兹海默病患者的组织中都发现了衰老细胞。在之前的研究中,清除衰老细胞(Senolysis疗法)是一种非常有前景的抗衰老治疗策略,可以改善与小鼠衰老有关的正常和病理变化。然而,大多数抗衰老药物都会抑制抗凋亡途径,这就产生了对正常组织的副作用。所以科研人员一直在寻找没有副作用新的Senolytics疗法。
近日,来自日本的众多研究机构在国际期刊Nature Aging上发表了题为“Senolytic vaccination improves normal andpathological age-related phenotypes and increases lifespan in progeroid mice”的研究成果。该研究小组描述了他们开发的疫苗是如何起作用的以及它在用于测试小鼠时的效果。研究表明基于糖蛋白非转移性黑色素瘤蛋白B(GPNMB)衰老抗原开发的多肽疫苗,可以选择性清除衰老细胞,改善正常和病理性的衰老相关症状,并延长了早衰小鼠的寿命,尤其是雄性小鼠。

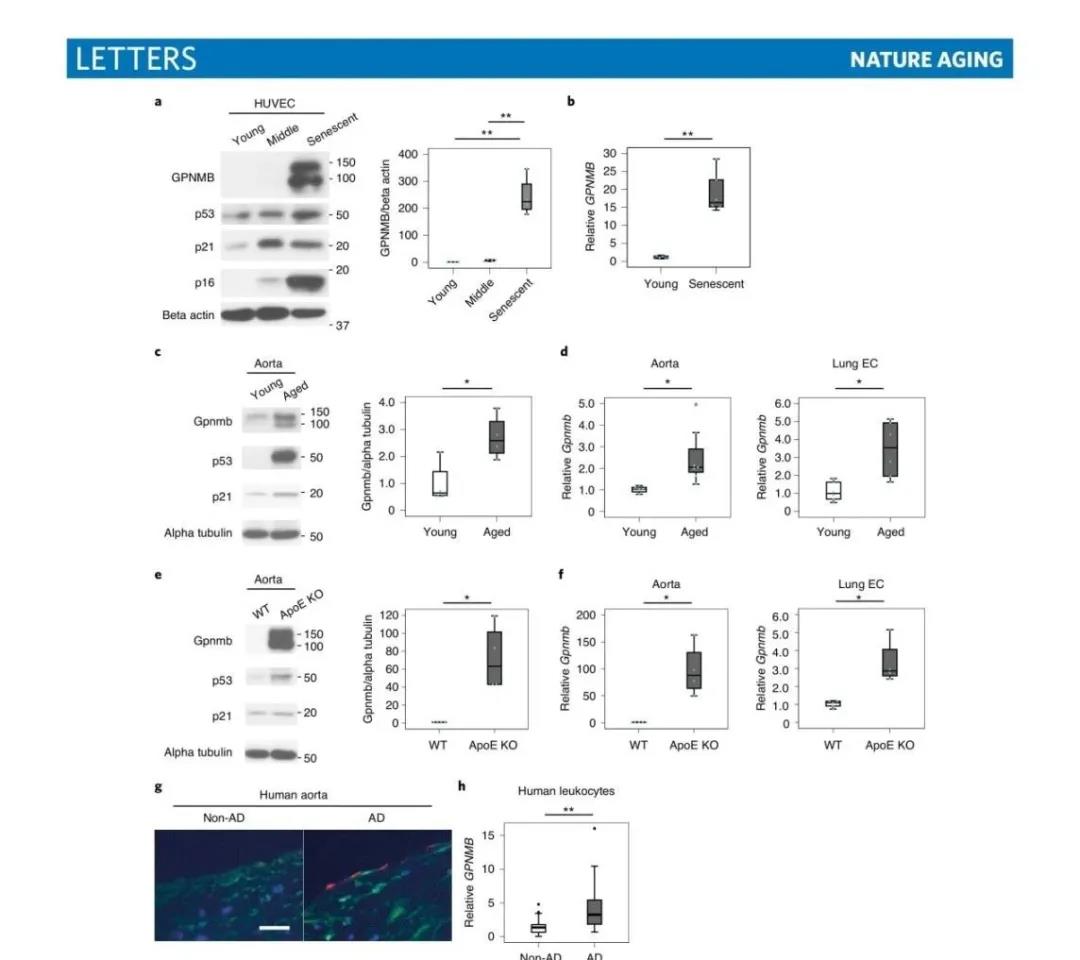
为了开发一种更有针对性的、减少脱靶效应的衰老细胞清除疗法,研究人员使用衰老的人血管内皮细胞转录组数据来寻找具有跨膜结构域的蛋白。通过使用数据分析工具GEO2R和蛋白质的跨膜分析软件TMHMM2.0,推测了10个存在跨膜区域的基因。在这些基因中,研究人员选择GPNMB作为候选的seno-抗原基因。因为研究人员在进一步的研究发现,在复制性衰老的人脐静脉内皮细胞(HUVECs)中,GPNMB的表达显著增加。研究人员还发现,在老龄小鼠、载脂蛋白E被敲除的小鼠和高脂饮食小鼠(HFD)的主动脉和隔离内皮细胞中,GPNMB的表达显著上调,并显示这种上调与衰老标志物的表达增加有关,比如p53和p21。此外,GPNMB在老年小鼠的其他组织也有上调现象,比如肺、内脏脂肪和骨髓,以及HFD喂养的小鼠的内脏脂肪中。组织学检查显示,GPNMB在动脉粥样硬化患者的血管内皮细胞中表达上调,但在无动脉粥样硬化患者的细胞中没有上调。同样,与无动脉粥样硬化患者的白细胞相比,动脉粥样硬化患者的白细胞中GPNMB的表达也明显增加。这些结果表明,GPNMB可能是用于衰老治疗的一个分子靶点。
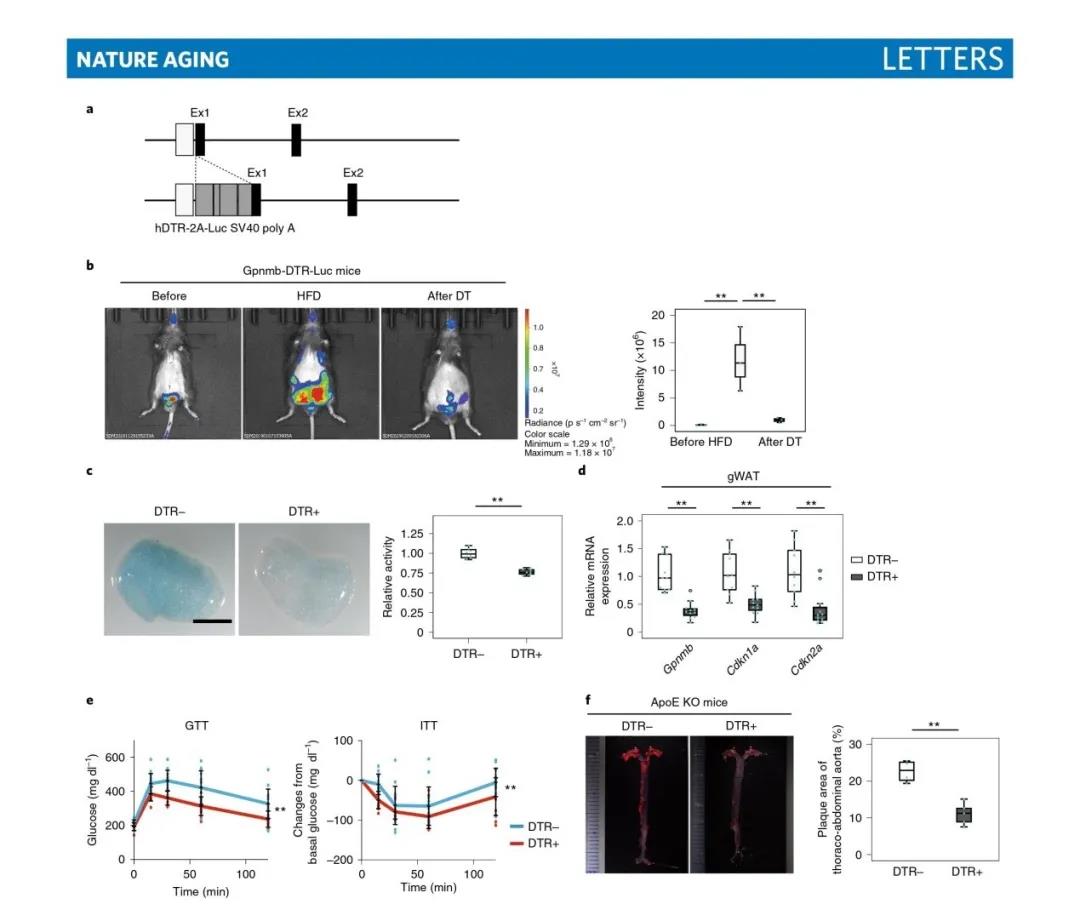
为了探究GPNMB作为衰老治疗的分子靶点的可能性,研究人员建立了转基因小鼠模型,其中白喉毒素受体(DTR)和荧光素酶在Gpnmb基因位点表达(Gpnmb-DTR-荧光素酶小鼠),这样可以使研究人员能够通过监测荧光素酶活性来检测Gpnmb阳性细胞并通过给予白喉毒素(DT)消除这些细胞。Gpnmb-DTR-荧光素酶小鼠在4至16周龄时以高脂饲料喂养,在12和14周时腹腔注射DT。研究结果与研究人员对HFD小鼠内脏脂肪中Gpnmb表达的western blot分析一致,在16周时对Gpnmb-DTR-荧光素酶小鼠进行分析,在腹部检测到强烈的荧光素酶信号。相反,给与DT会降低腹部的荧光素酶活性,这种降低与内脏脂肪组织衰老样变化的改善有关,比如衰老相关的β-半乳糖酶(SA-β-gal)活性的降低以及Cdkn2a和Cdkn1a表达的下调说明了这一点。Gpnmb阳性细胞的缺失也明显改善了HFD所引起的代谢异常。此外,研究人员建立了具有载脂蛋白E 被敲除的Gpnmb-DTR-荧光素酶小鼠模型,研究结果显示,Gpnmb阳性细胞的缺失明显减少了动脉粥样硬化斑块的负担,这进一步证明了GPNMB可能是衰老治疗的分子靶点。
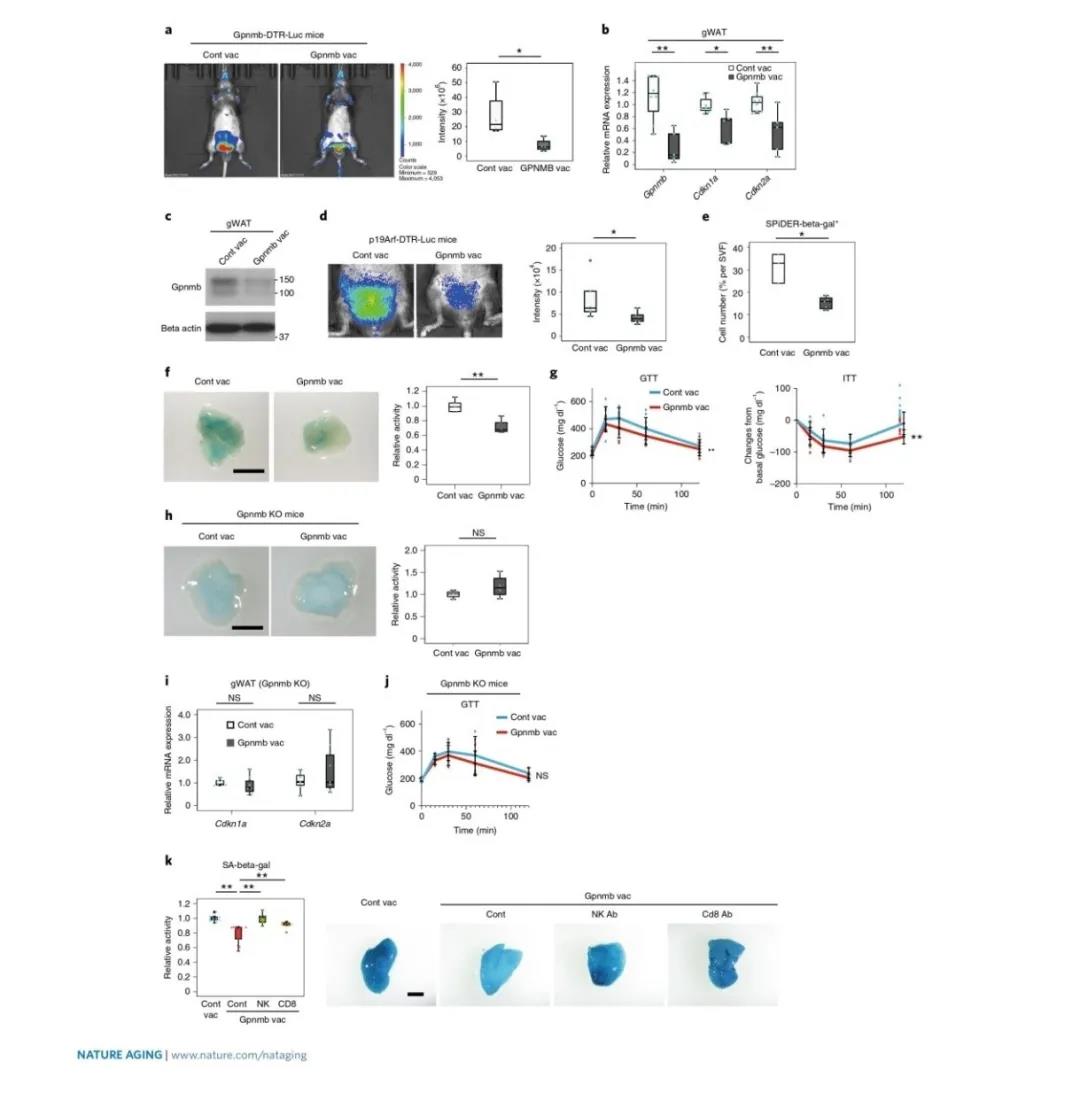
接下来,研究人员开发了一种Gpnmb的多肽疫苗,以进一步探索接种GPNMB疫苗对HFD小鼠代谢异常的影响。小鼠从4周龄开始喂养高脂饮食,并在8周龄时通过皮下注射Gpnmb疫苗进行免疫,随后在16周时进行检测分析。研究结果显示,疫苗减少了Gpnmb的表达和内脏脂肪组织中相关的荧光素酶活性,表明这种疫苗消除了Gpnmb阳性细胞。此外,接种Gpnmb疫苗还能减弱p19Arf依赖的荧光素酶活性增加,并显著改善内脏脂肪组织中衰老样表型变化(SA-beta-gal活性的增加和细胞周期负调控因子的上调),与给予对照疫苗的小鼠相比,明显改善了代谢状况。然而,当研究人员给Gpnmb敲除的小鼠注射Gpnmb疫苗时,却没有观察到这些效果,表明疫苗产生的效应是由Gpnmb介导的。此外,当对接种的小鼠进行抗NK或CD8+T细胞的中和抗体处理时,Gpnmb疫苗的有益影响减弱,表明NK和CD8+ T细胞对Gpnmb疫苗在体内的效应至关重要。
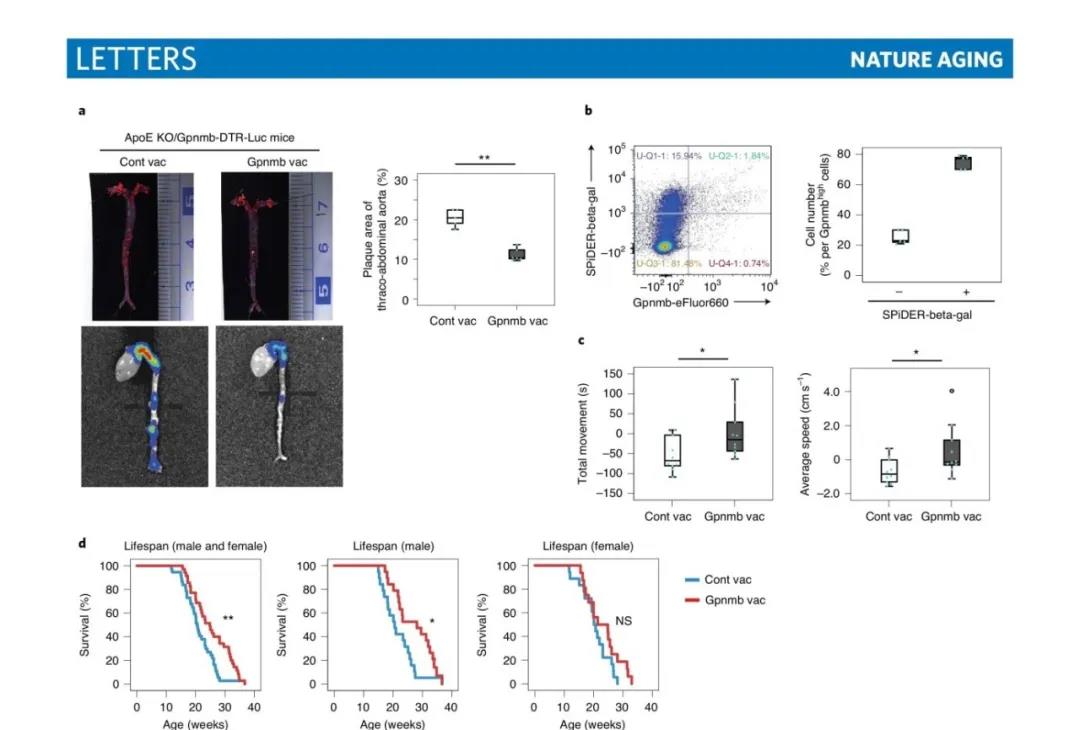
在另一个实验中,研究人员从4周龄开始给载脂蛋白E 被敲除的小鼠喂食HFD,在8周龄时注射Gpnmb疫苗,随后在16周时进行检测分析。研究结果显示,与对照疫苗相比,注射Gpnmb疫苗可明显减少动脉粥样硬化,并降低主动脉中依赖Gpnmb的荧光素酶活性。主动脉中促炎症分子的表达因Gpnmb疫苗接种而下调,同时Gpnmb和细胞周期阴性调节剂的表达也减少。
为了研究接种疫苗对正常衰老的影响,研究人员给中年小鼠(50周龄)注射了Gpnmb疫苗,并在接种疫苗后20周(70周龄)时进行实验分析。研究结果显示,在对照组中小鼠总运动量和平均运动速度都随着年龄的增长而下降,但这些与年龄相关的这些变化在接种Gpnmb疫苗后得到了明显的改善。为了进一步探索Gpnmb疫苗对寿命的影响,研究人员在10周龄时给Zmpste24敲除小鼠(早衰症模型)接种疫苗,并评估其存活率。研究结果显示,在对照组中,所有的老鼠都在30周龄的时候死亡。相比之下,小鼠尤其是雄性小鼠,接种Gpnmb疫苗后其存活率更高。同样,与对照组小鼠相比,注射Gpnmb疫苗显著延长了Zmpste24敲除小鼠的中位寿命(雄性小鼠21.7±1.27周vs 27.1±1.53周;雌性小鼠20.5±1.13周vs 23.2±1.46周)。
先前的研究已经验证了20多种药物,它们都能选择性地清除衰老细胞。其中,达沙替尼和槲皮素(D+Q)这两种衰老剂的组合,已被证明能明显改善老年小鼠的血管舒缩功能,并缓解肥胖引起的代谢功能障碍。此外,Navitoclax(ABT-263)已被证明可以改善葡萄糖代谢和β细胞功能,同时减少衰老标志物和SASP因子的表达。
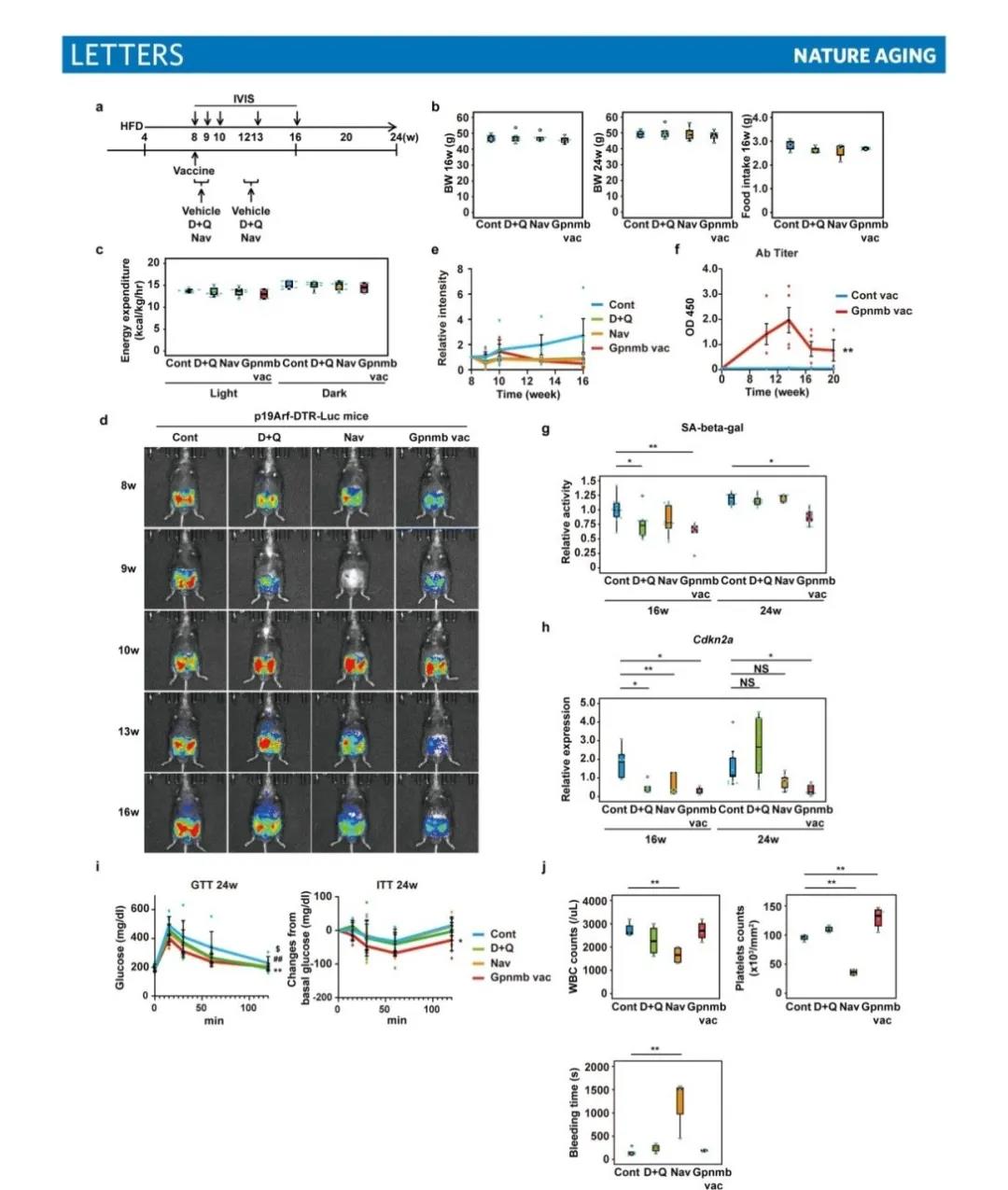
研究人员比较了Gpnmb疫苗接种与D+Q和Navitoclax治疗对小鼠的影响。研究结果显示,用D+Q或Navitoclax治疗组,p19Arf依赖的荧光素酶活性的增加在腹部被削弱。同样,Gpnmb疫苗接种抑制了p19Arf依赖性荧光素酶活性的增加,同时抗Gpnmb抗体的滴度增加。此外,内脏脂肪组织中衰老样表型变化(SA-beta-gal活性的增加和Cdkn2a的上调),小鼠16周龄时在D + Q和Navitoclax组中得到改善,然而这些有益的影响在24周龄时下降了。相反,Gpnmb疫苗接种组持续改善了内脏脂肪组织的衰老样表型变化。用D+Q或Navitoclax治疗可改善葡萄糖不耐受,但24周龄时出现了胰岛素抵抗。相反,Gpnmb疫苗接种组对糖代谢的有利影响持续到24周龄。
总之,在这项研究中,研究人员开发的衰老疫苗改善了与衰老有关的正常和病理性的衰老相关症状,并延长了早衰小鼠的寿命。研究人员表示,这是一项令人兴奋的研究,因为该研究可能为Senolytics疗法提供一种全新的策略。



