相信大家都发现了,如今肥胖的人越来越多。致肥胖饮食(又称"西方饮食")脂肪含量高,糖含量高,比如我们常吃的汉堡、薯条、披萨。但是,吃进去的可不是美食,是肥胖!
潘氏细胞,又称帕内特细胞,Paneth细胞,是小肠腺的特征性细胞,可以分泌抗菌肽,对于肠道先天免疫至关重要。研究表明,在小鼠中潘氏细胞功能异常会引起黏膜功能障碍,导致克罗恩病的发生。因此,潘氏细胞缺陷或功能障碍可能是炎症性肠病的病因。潘氏细胞功能正常是肠道中抗炎的关键。肥胖是否会影响潘氏细胞的功能,目前尚未可知。
2021年5月18日,来自华盛顿大学医学院病理与免疫学系的研究人员在《Cell Host & Microbe》上发表了题为Western diet induces Paneth cell defects through microbiome alterations and farnesoid X receptor and type I interferon activation的研究成果。该研究发现,西方饮食通过依赖于微生物组和法尼醇X受体(FXR)和I型干扰素(IFN)信号传导的机制导致Paneth细胞功能障碍。并且,肥胖与Paneth细胞功能障碍有关。

西方饮食通过依赖于微生物组和法尼醇X受体(FXR)和I型干扰素(IFN)信号传导的机制导致Paneth细胞功能障碍
为了排除其他生活方式或环境因素对潘氏细胞的影响,研究人员使用潘氏细胞表型个体库(现在有930种来自多种疾病的个体)来搜索与潘氏细胞表型异常相关的其他特征。结果表明潘氏细胞异常的百分比与体重指数升高之间存在相关性,也就是说,超重和肥胖的人容易出现潘氏细胞缺陷。
随后,研究人员将西方饮食喂养的小鼠出现潘氏细胞缺陷,并且,这种功能缺陷是可逆的。
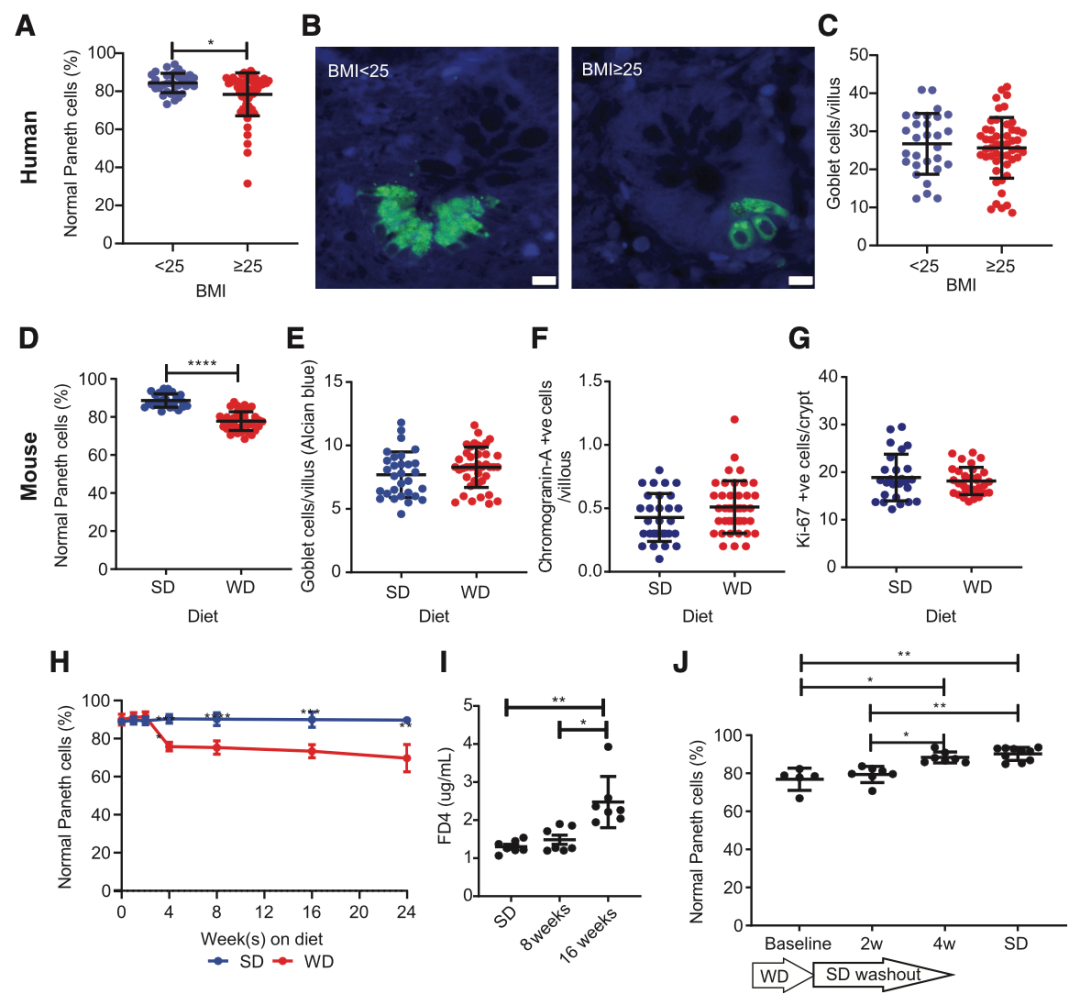
在人类和小鼠中,肥胖与Paneth细胞功能障碍有关
研究人员为了确定西方饮食诱导的潘氏细胞缺陷的分子机制,对西方饮食和正常饮食的小鼠的全层小肠进行RNA-seq分析。结果表明,与FXR激活相关的基因与西方饮食喂养密切相关。此外,在非IBD且BMI大于25的受试者的回肠标本中,与激活FXR通路相关的基因mRNA表达升高。
更重要的是,通过药物激活FXR可特异性抑制与潘氏细胞功能相关的基因。并且,研究人员还发现西方饮食喂养的小鼠回肠中IFN刺激的基因表达增强,血清中I型IFN生物活性升高。这些结果表明,西方饮食的小鼠中潘氏细胞缺陷与激活的FXR和I型IFN信号传导有关。过量的FXR活化可激活I型IFN,直接介导肠道上皮中潘氏细胞缺陷。
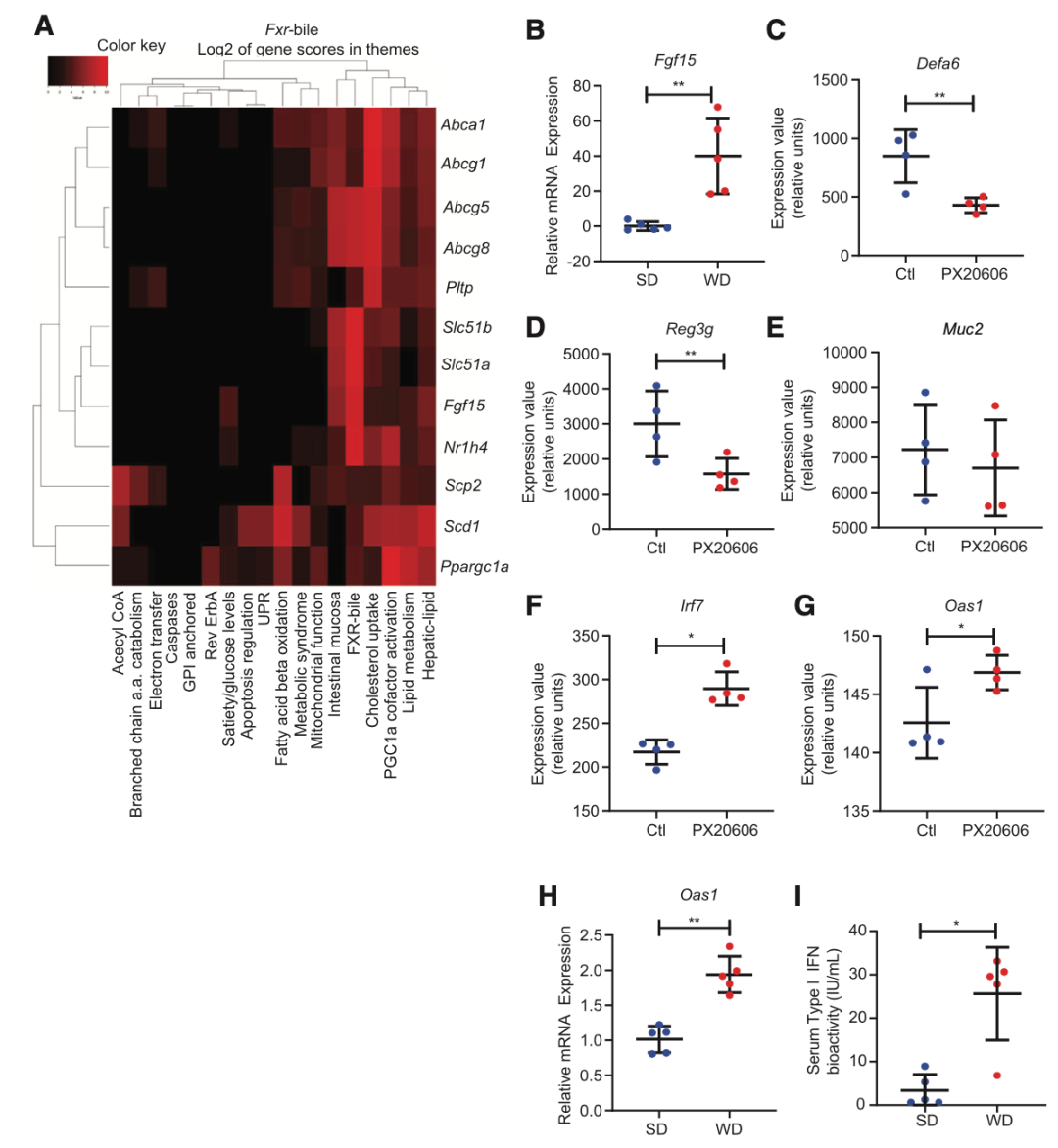
西方饮食的小鼠中Paneth细胞缺陷与激活的FXR和I型IFN信号传导有关
另外,研究人员发现,在小鼠中使用FXR激动剂处理,可增加沙门氏菌的死亡率;而FXR敲除小鼠中,沙门氏菌的死亡率显著降低。通过质谱分析小肠中的胆汁酸胆酸、鹅去氧胆酸、多酚酸、伯胆汁酸和石胆酸的水平,发现西方饮食喂养的小鼠中,潘氏细胞缺陷可诱导伯胆汁酸和石胆酸显著增加,其中微生物可促进胆汁酸转化。
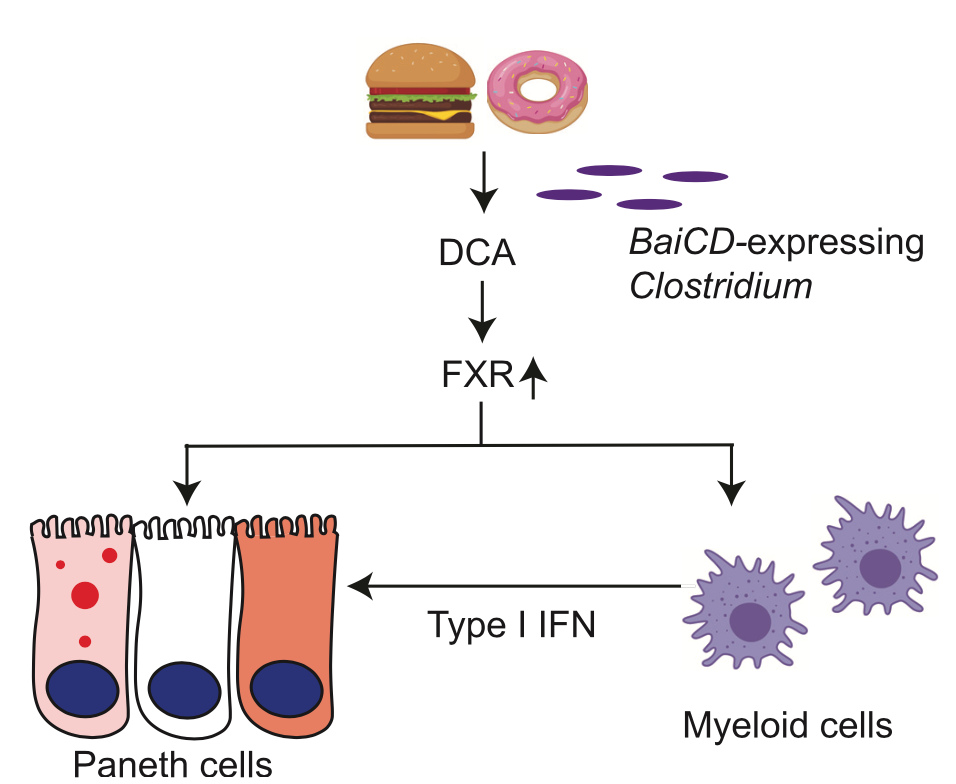
西方饮食诱导Paneth细胞功能缺陷模式图
简而言之,研究表明长期食用富含脂肪和糖的西方饮食会损害肠道免疫细胞的功能,从而促进炎症性肠病或增加肠道感染的风险。研究人员表示,他们正在研究如何通过靶向胆汁酸或FXR/I型IFN来恢复潘氏细胞的功能;但是习惯吃西餐的人是否可以通过改变饮食方式来提高肠道免疫力仍有待进一步的研究。肥胖不是一夜吃成的,为了健康,放下手中的披萨吧!



