抗生素类药物曾是人类对抗诸多疾病的“秘密武器”,但由于细菌对抗生素耐药性的不断增强,抗生素逐渐走下了“神坛”,为此亟需不断寻求新的方法来应对细菌感染。
近日,《Plos Pathogens》杂志发表了一篇题为UPEC kidney infection triggers neuro-immune communication leading to modulation of local renal inflammation by splenic IFNγ的文章,揭示了神经系统感知局部细菌感染并迅速激活免疫反应的新机制。

在传统印象里,神经系统只是信息的接收者和传递者,然而它其实并没有如此“单纯”。新研究发现,当遭遇细菌侵袭后,人体神经组织就会启动 “感知和警报”系统,在感染数小时内将预警信息快马加鞭的递送给身体各组织器官。
为了提供神经系统“雷厉风行”的有效证据,科研人员构建了高度技术性的体内感染模型,分析了肾脏感染触发脾脏感染的连锁反应时间。发现在肾脏发生尿毒症性大肠杆菌(UPEC)感染的4小时内,就会在脾脏会触发IFNγ反应。
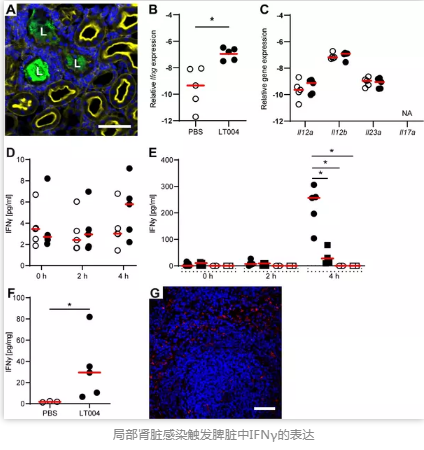
然而有趣的是,研究数据或暗示,由肾脏感染触发的器官间的相互通讯可能不受典型的体液炎症途径驱动,这激发了研究人员对其他信号传导途径的兴趣:脾脏到底是如何如此迅速地知道肾脏被感染的呢?
研究人员对肾脏中的感觉神经进行了染色后发现,肾脏被细菌感染后,一种细菌所表达的特定毒素“alpha-溶血素”就会直接或间接的激活神经元,导致脾脏中IFN gamma增加,并使UPEC感染的肾上皮细胞产生炎症信号,从而利用脾神经将信息传送至脾脏。
研究人员对肾脏中的感觉神经进行了染色后发现,肾脏被细菌感染后,一种细菌所表达的特定毒素“alpha-溶血素”就会直接或间接的激活神经元,导致脾脏中IFN gamma增加,并使UPEC感染的肾上皮细胞产生炎症信号,从而利用脾神经将信息传送至脾脏。
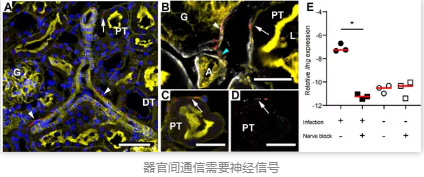
接下来,研究人员想一探细菌性肾脏感染激活感觉神经系统的确切分子机制到底为何。
早期研究发现,UPEC 外毒素α-溶血素(HlyA)可在体内表达,并会对肾脏感染的早期动力学产生影响。为此,研究人员分离了原代背根神经节(DRG)细胞,并用UPEC菌株LT004直接感染DRG细胞。
研究发现 HlyA可以通过直接刺激神经免疫轴,或通过感染肾上皮细胞释放胞外ATP(eATP)间接触发全身性免疫调节反应。因此HlyA的表达对于细菌感染后触发肾脏和脾脏之间神经驱动很重要。
研究发现 HlyA可以通过直接刺激神经免疫轴,或通过感染肾上皮细胞释放胞外ATP(eATP)间接触发全身性免疫调节反应。因此HlyA的表达对于细菌感染后触发肾脏和脾脏之间神经驱动很重要。
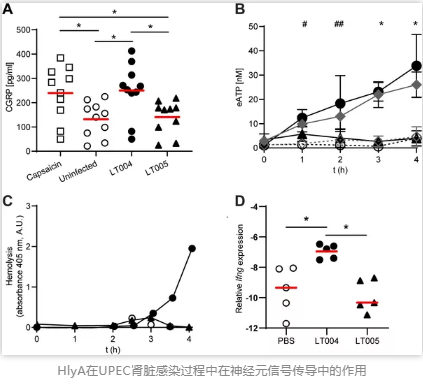
在细菌感染早期,作为免疫监视与免疫调节反应的传令兵,神经系统功不可没。这项研究充分突出了神经系统在细菌感染早期的重要性。在后抗生素时代,通过神经系统调控细菌感染或能成为检测或控制感染的一种新方式。



