摘要:第一个表明RAS基因突变可以以一种全新的方式促进癌症的研究
美国国立卫生研究院(NIH)的科学家和合作者表示,他们发现了一种新的途径,即RAS基因(在癌症中常见的突变)可能会推动肿瘤生长,而不是在细胞表面发挥众所周知的信号传导作用。
根据研究人员在Nature Cancer上发表的“The pro-oncogenic noncanonical activity of a RAS•GTP:RanGAP1 complex facilitates nuclear protein export”的研究,突变的RAS有助于启动一系列涉及特定核蛋白运输的事件,从而导致不受控制的肿瘤生长。

图1 RanGAP1复合物促进核蛋白输出
RAS基因是癌症中第二常见的突变基因,突变的RAS蛋白是一些最致命癌症的关键驱动因素,包括几乎所有的胰腺癌、一半的结直肠癌和三分之一的肺癌。几十年的研究表明,突变的RAS蛋白通过激活细胞表面的特定蛋白质来促进肿瘤的发育和生长,从而产生一个持续的信号流,告诉细胞生长
“这是第一个研究表明突变的RAS基因可以以一种全新的方式促进癌症,”研究作者、美国国立卫生研究院国家癌症研究所(NCI)副主任Douglas Lowy博士说。“RAS蛋白的额外作用的发现对改善治疗具有令人兴奋的意义。”
应用于治疗RAS引发的癌症
研究人员认为,他们的工作可能在治疗RAS引发的癌症方面有潜在的应用。他们已经开始研究RAS的功能在胰腺癌中的作用,特别是因为这种类型的癌症很少有有效的治疗方法。
阻断突变RAS蛋白的药物被用作癌症治疗只有几年的时间,并且已经被FDA批准用于治疗肺癌和肉瘤。尽管RAS抑制剂的开发取得了重大的科学成功,但迄今为止,RAS抑制剂对患者预后的影响有限,大多数患者的生存期仅提高了几个月。
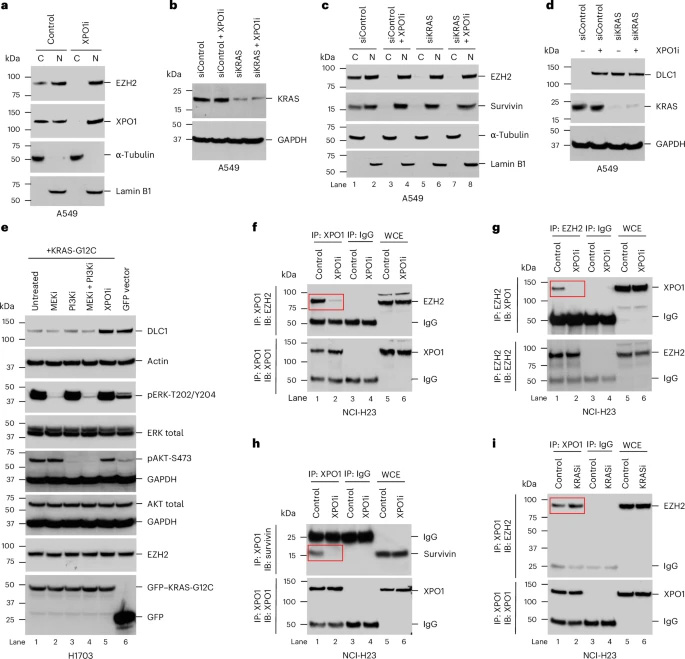
图2 RAS独立于PI3K和MEK信号传导调节核蛋白输出
35年前,由Lowy领导的一个小组进行了早期研究,确定RAS是一种致癌基因,并帮助解释了它是如何促进肿瘤生长的。在这项新的研究中,研究小组发现突变体RAS直接参与了核蛋白EZH2从细胞核转运到细胞质的过程。一旦被释放,EZH2就会促进一种叫做DLC1的肿瘤抑制蛋白的分解。阻断突变体RAS阻止EZH2的释放,恢复DLC1的活性。
在人类肺癌细胞系和小鼠肺癌模型的实验中,研究人员发现,将RAS抑制剂与不同的靶向癌症药物联合使用,重新激活DLC1的肿瘤抑制活性,具有强大的抗癌活性-比单独使用RAS抑制剂更有效。
该研究还发现,突变的RAS蛋白在其他类型的癌症中也具有相同的功能,这表明这种机制可能是RAS基因突变的癌症的普遍特征。
“考虑到RAS的新作用,有一天可能会开发出新的治疗组合,”Lowy说。
参考资料
[1] The pro-oncogenic noncanonical activity of a RAS•GTP:RanGAP1 complex facilitates nuclear protein export
摘要:第一个表明RAS基因突变可以以一种全新的方式促进癌症的研究
美国国立卫生研究院(NIH)的科学家和合作者表示,他们发现了一种新的途径,即RAS基因(在癌症中常见的突变)可能会推动肿瘤生长,而不是在细胞表面发挥众所周知的信号传导作用。
根据研究人员在Nature Cancer上发表的“The pro-oncogenic noncanonical activity of a RAS•GTP:RanGAP1 complex facilitates nuclear protein export”的研究,突变的RAS有助于启动一系列涉及特定核蛋白运输的事件,从而导致不受控制的肿瘤生长。

图1 RanGAP1复合物促进核蛋白输出
RAS基因是癌症中第二常见的突变基因,突变的RAS蛋白是一些最致命癌症的关键驱动因素,包括几乎所有的胰腺癌、一半的结直肠癌和三分之一的肺癌。几十年的研究表明,突变的RAS蛋白通过激活细胞表面的特定蛋白质来促进肿瘤的发育和生长,从而产生一个持续的信号流,告诉细胞生长
“这是第一个研究表明突变的RAS基因可以以一种全新的方式促进癌症,”研究作者、美国国立卫生研究院国家癌症研究所(NCI)副主任Douglas Lowy博士说。“RAS蛋白的额外作用的发现对改善治疗具有令人兴奋的意义。”
应用于治疗RAS引发的癌症
研究人员认为,他们的工作可能在治疗RAS引发的癌症方面有潜在的应用。他们已经开始研究RAS的功能在胰腺癌中的作用,特别是因为这种类型的癌症很少有有效的治疗方法。
阻断突变RAS蛋白的药物被用作癌症治疗只有几年的时间,并且已经被FDA批准用于治疗肺癌和肉瘤。尽管RAS抑制剂的开发取得了重大的科学成功,但迄今为止,RAS抑制剂对患者预后的影响有限,大多数患者的生存期仅提高了几个月。

图2 RAS独立于PI3K和MEK信号传导调节核蛋白输出
35年前,由Lowy领导的一个小组进行了早期研究,确定RAS是一种致癌基因,并帮助解释了它是如何促进肿瘤生长的。在这项新的研究中,研究小组发现突变体RAS直接参与了核蛋白EZH2从细胞核转运到细胞质的过程。一旦被释放,EZH2就会促进一种叫做DLC1的肿瘤抑制蛋白的分解。阻断突变体RAS阻止EZH2的释放,恢复DLC1的活性。
在人类肺癌细胞系和小鼠肺癌模型的实验中,研究人员发现,将RAS抑制剂与不同的靶向癌症药物联合使用,重新激活DLC1的肿瘤抑制活性,具有强大的抗癌活性-比单独使用RAS抑制剂更有效。
该研究还发现,突变的RAS蛋白在其他类型的癌症中也具有相同的功能,这表明这种机制可能是RAS基因突变的癌症的普遍特征。
“考虑到RAS的新作用,有一天可能会开发出新的治疗组合,”Lowy说。
参考资料
[1] The pro-oncogenic noncanonical activity of a RAS•GTP:RanGAP1 complex facilitates nuclear protein export



