摘要:一项临床前研究,可能很快就可以确定哪些肝癌患者会从免疫治疗中受益。
根据威尔康奈尔医学研究人员的一项临床前研究,可能很快就可以确定哪些肝癌患者会从免疫治疗中受益。
这项研究发表在10月17日的《分子细胞》(Molecular Cell)杂志上,为一对名为p62和NBR1的蛋白质提供了新的见解,以及它们在调节肝星状细胞干扰素反应中的相反功能,肝星状细胞是肝脏对抗肿瘤的关键免疫成分。该研究表明,这些特化细胞中高水平的免疫抑制NBR1可能会识别出不太可能对免疫疗法产生反应的患者。该研究还表明,在动物模型中,降低nbr1的策略有助于缩小肿瘤,这为那些对免疫治疗无反应的患者提供了一种潜在的新治疗方法。

图1 NBR1和p62对肝星状细胞STING通路的反向调节决定了肝细胞癌的进展
Jorge Moscat博士说:“P62和NBR1是阴阳。与NBR1相反,如果p62在肝星状细胞中含量高,患者就不会患癌症,但如果p62含量低,免疫系统就会被破坏。如果NBR1高,免疫系统就会受损,但如果NBR1低,免疫反应就会增强。”
直到最近,肝细胞癌患者几乎没有治疗选择,而那些可用的治疗只能延长几个月的生命。免疫疗法为这些患者提供了一种新的选择,并可能延长他们的生命长达两年。
“肝脏是一个免疫功能受到极大抑制的器官,”联合首席研究员Maria Diaz-Meco博士说。“重新激活免疫系统是一种非常有吸引力的方法,现在正在取得成果。”
然而,并非所有患者对免疫疗法都有反应,只有一小部分患者实现了长期缓解。临床医生目前无法预测哪些患者会受益。她说:“我们需要生物标志物来确定哪些患者会有反应,哪些患者会获得长期生存。”
Drs Moscat和Diaz-Meco与共同第一作者Sadaaki Nishimura博士和Juan F. Linares博士(分别是威尔康奈尔医学院病理学和实验室医学系的博士后和讲师)以及Antoine L'Hermitte博士(前Sanford Burnham Prebys医学发现研究所)合作进行了这项研究。
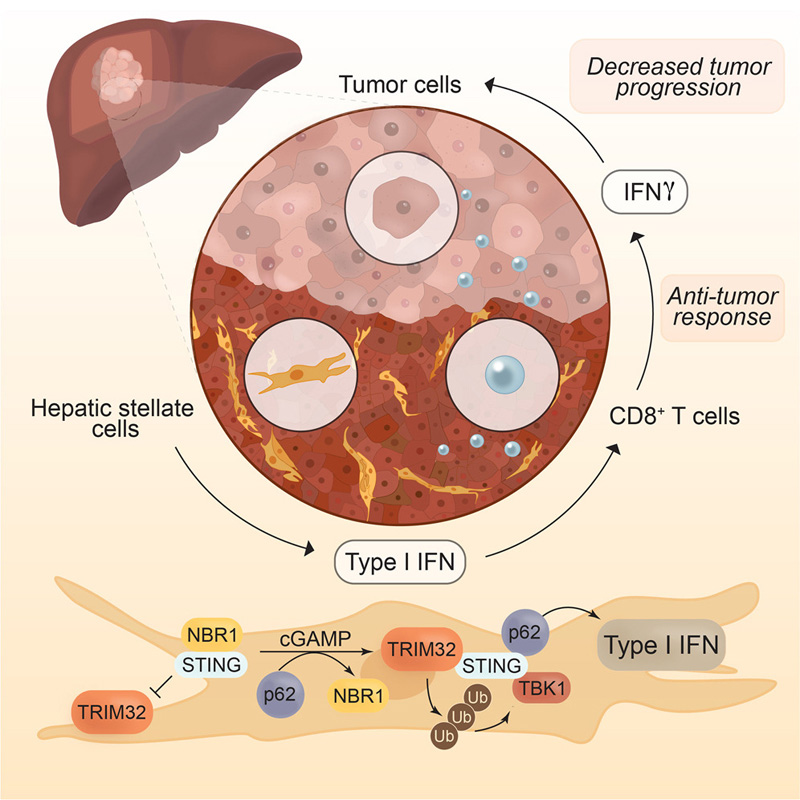
图2 p62通过促进HSC中第三方基序蛋白32(TRIM32)的STING泛素化来激活干扰素(IFN)级联
研究人员旨在通过研究导致癌症的肝脏愈合机制中出现的问题来确定生物标志物和潜在的治疗靶点。先前的研究发现,在肝癌患者中,肿瘤抑制蛋白p62的水平不可逆转地降低。这项新研究表明,通常情况下,p62通过激活一种叫做STING的蛋白质来促进免疫反应,这种蛋白质会将NBR1推开,引发一种破坏肿瘤细胞的免疫反应。相比之下,NBR1促进STING的分解并阻断免疫反应。从肝细胞癌小鼠的肝星状细胞中删除NBR1,即使p62水平保持在低水平,也能恢复免疫反应并缩小肿瘤。
该团队目前正在研究如何开发一种疗法,使患者体内的NBR1降解,并阻止其与STING相互作用。目标是重新激活免疫系统,帮助提高免疫治疗的有效性。激活STING的药物也在开发中,可能会提供另一种方法来帮助增强肝细胞癌患者的免疫反应。该团队还将研究敲除NBR1是否有助于防止多种癌症的转移或防止肿瘤对治疗产生耐药性。
Moscat和Diaz-Meco博士计划继续研究调节肝脏免疫反应的途径。
“如果我们不能完全理解调节这些过程的分子机制,免疫疗法就不会取得进展,我们也无法理解为什么它对一些病人有效,而对另一些病人无效,”Diaz-Meco博士说。
参考资料
[1] Opposing regulation of the STING pathway in hepatic stellate cells by NBR1 and p62 determines the progression of hepatocellular carcinoma
摘要:一项临床前研究,可能很快就可以确定哪些肝癌患者会从免疫治疗中受益。
根据威尔康奈尔医学研究人员的一项临床前研究,可能很快就可以确定哪些肝癌患者会从免疫治疗中受益。
这项研究发表在10月17日的《分子细胞》(Molecular Cell)杂志上,为一对名为p62和NBR1的蛋白质提供了新的见解,以及它们在调节肝星状细胞干扰素反应中的相反功能,肝星状细胞是肝脏对抗肿瘤的关键免疫成分。该研究表明,这些特化细胞中高水平的免疫抑制NBR1可能会识别出不太可能对免疫疗法产生反应的患者。该研究还表明,在动物模型中,降低nbr1的策略有助于缩小肿瘤,这为那些对免疫治疗无反应的患者提供了一种潜在的新治疗方法。

图1 NBR1和p62对肝星状细胞STING通路的反向调节决定了肝细胞癌的进展
Jorge Moscat博士说:“P62和NBR1是阴阳。与NBR1相反,如果p62在肝星状细胞中含量高,患者就不会患癌症,但如果p62含量低,免疫系统就会被破坏。如果NBR1高,免疫系统就会受损,但如果NBR1低,免疫反应就会增强。”
直到最近,肝细胞癌患者几乎没有治疗选择,而那些可用的治疗只能延长几个月的生命。免疫疗法为这些患者提供了一种新的选择,并可能延长他们的生命长达两年。
“肝脏是一个免疫功能受到极大抑制的器官,”联合首席研究员Maria Diaz-Meco博士说。“重新激活免疫系统是一种非常有吸引力的方法,现在正在取得成果。”
然而,并非所有患者对免疫疗法都有反应,只有一小部分患者实现了长期缓解。临床医生目前无法预测哪些患者会受益。她说:“我们需要生物标志物来确定哪些患者会有反应,哪些患者会获得长期生存。”
Drs Moscat和Diaz-Meco与共同第一作者Sadaaki Nishimura博士和Juan F. Linares博士(分别是威尔康奈尔医学院病理学和实验室医学系的博士后和讲师)以及Antoine L'Hermitte博士(前Sanford Burnham Prebys医学发现研究所)合作进行了这项研究。

图2 p62通过促进HSC中第三方基序蛋白32(TRIM32)的STING泛素化来激活干扰素(IFN)级联
研究人员旨在通过研究导致癌症的肝脏愈合机制中出现的问题来确定生物标志物和潜在的治疗靶点。先前的研究发现,在肝癌患者中,肿瘤抑制蛋白p62的水平不可逆转地降低。这项新研究表明,通常情况下,p62通过激活一种叫做STING的蛋白质来促进免疫反应,这种蛋白质会将NBR1推开,引发一种破坏肿瘤细胞的免疫反应。相比之下,NBR1促进STING的分解并阻断免疫反应。从肝细胞癌小鼠的肝星状细胞中删除NBR1,即使p62水平保持在低水平,也能恢复免疫反应并缩小肿瘤。
该团队目前正在研究如何开发一种疗法,使患者体内的NBR1降解,并阻止其与STING相互作用。目标是重新激活免疫系统,帮助提高免疫治疗的有效性。激活STING的药物也在开发中,可能会提供另一种方法来帮助增强肝细胞癌患者的免疫反应。该团队还将研究敲除NBR1是否有助于防止多种癌症的转移或防止肿瘤对治疗产生耐药性。
Moscat和Diaz-Meco博士计划继续研究调节肝脏免疫反应的途径。
“如果我们不能完全理解调节这些过程的分子机制,免疫疗法就不会取得进展,我们也无法理解为什么它对一些病人有效,而对另一些病人无效,”Diaz-Meco博士说。
参考资料
[1] Opposing regulation of the STING pathway in hepatic stellate cells by NBR1 and p62 determines the progression of hepatocellular carcinoma



