摘要:研究人员现在发现,已知会增加一个人患糖尿病风险的DNA序列变化与胰腺细胞处理两种不同分子压力的能力有关。
胰腺细胞和人一样,只能承受一定的压力,然后就会开始崩溃。某些压力源,如炎症和高血糖,会使这些细胞不堪重负,从而导致2型糖尿病的发展。
杰克逊实验室(JAX)的研究人员现在发现,已知会增加一个人患糖尿病风险的DNA序列变化与胰腺细胞处理两种不同分子压力的能力有关。在有这些DNA变化的人身上,胰腺中产生胰岛素的细胞在暴露于压力和炎症时可能更容易衰竭或死亡。
JAX副教授Michael L. Stitzel和JAX教授Dugyu Ucar共同撰写了这项新研究,该研究发表在10月8日的《细胞代谢》高级在线版上,他说:“最终,我们希望通过针对最易患这种疾病的人的基因和途径,开发出预防和治疗2型糖尿病的新方法。”“这些发现让我们对其中一些基因和途径有了新的认识。”
这项工作指出了几十个与细胞压力和糖尿病风险有关的基因,其中一个基因已经在研究中,可以作为治疗2型糖尿病并发症的药物靶点。

图1 多组分人胰岛内质网和细胞因子应激反应图谱提供了2型糖尿病的遗传见解
压力下的细胞
当活细胞面临挑战,包括损伤、炎症或营养变化时,它们会激活保护性反应,试图应对和逆转压力。但随着时间的推移,持续的压力会压倒细胞,导致它们减缓或死亡。
在胰岛β细胞中,两种类型的细胞压力与2型糖尿病的发展有关。
内质网(ER)应激发生时,细胞变得不堪重负的高需求产生蛋白质,如胰岛素,以帮助调节血糖水平。
当免疫系统发出过多的炎症信号时,细胞因子压力就会发生——就像肥胖和代谢疾病一样。
在这两种情况下,压力最终会导致胰岛细胞停止产生胰岛素或死亡。
Stitzel和他的同事们想知道胰岛细胞使用了哪些基因和蛋白质来对内质网应激和细胞因子应激做出反应。
Stitzel说:“研究人员已经完成了多项研究,以了解哪些分子途径在调节快乐、健康的胰岛细胞的胰岛素分泌中起重要作用。”“但我们的假设是,胰岛细胞并不总是快乐的。那么,当细胞处于压力下时,哪些途径是重要的?我们每个人体内与糖尿病相关的DNA序列变化是如何影响它们的?”
应激反应的基因
Stitzel的研究小组将健康的人类胰岛细胞暴露于已知会引起内质网应激或细胞因子应激的化合物中。然后,他们追踪细胞中RNA分子水平的变化,以及细胞内不同DNA片段排列的紧密程度或松散程度——这是细胞在任何给定时间使用哪些基因和调控元件的代理。
为了分析结果,该团队与JAX的教授兼计算生物学家Ucar合作。科学家们共同发现,超过5000个基因,或健康胰岛细胞表达的所有基因的近三分之一,在内质网压力或细胞因子压力下改变了它们的表达。其中许多参与了蛋白质的产生,这对胰岛细胞产生胰岛素至关重要。大多数基因只参与一种或另一种应激反应,提出了两种不同的应激途径在糖尿病中起作用的观点。
此外,大约八分之一的用于胰岛细胞的DNA调节区域被压力改变。重要的是,这些调控区域中有86个先前被发现含有2型糖尿病高危人群的遗传变异。
Stitzel说:“这表明,具有这些基因变异的人的胰岛细胞对压力的反应可能比其他人更差。”“你的环境——比如糖尿病和肥胖——触发了2型糖尿病,但你的基因是扳机的扳机。”
Stitzel希望新的调控区域和基因列表最终能够通过潜在地使胰岛细胞更能适应压力而产生预防或治疗糖尿病的新药。
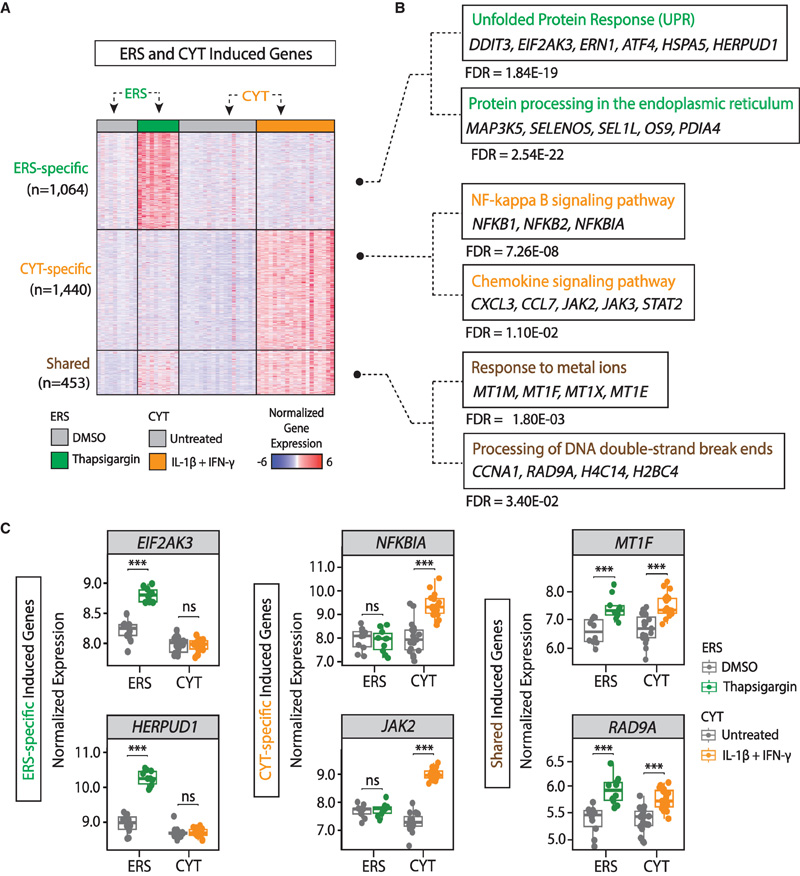
图2 人胰岛ER应激和细胞因子反应基因的综合比较图谱
一个可用药的目标
研究人员找到了一个被内质网应激改变的基因。该基因被称为MAP3K5,在胰岛素编码基因中含有引起糖尿病的突变的小鼠中,被证明可以改变胰岛β细胞的死亡。
在这篇新论文中,Stitzel和他的同事们表明,更高水平的MAP3K5导致更多的胰岛β细胞在内质网应激下死亡。另一方面,消除或阻断MAP3K5使胰岛细胞对内质网应激更有弹性,更不容易死亡。
针对MAP3K5的药物Selonsertib的早期研究表明,它可以降低糖尿病严重并发症的风险。新的研究结果指出了这种药物的另一个可能的作用——在糖尿病高危人群中预防糖尿病,帮助他们的胰岛细胞在细胞压力下保持功能和活力。
Stitzel说:“这种治疗方法已经在临床试验中,这确实令人兴奋,但要了解这种药物是否能够用于初级预防,还需要做更多的工作。”
参考资料
[1] Multi-omic human pancreatic islet endoplasmic reticulum and cytokine stress response mapping provides type 2 diabetes genetic insights
摘要:研究人员现在发现,已知会增加一个人患糖尿病风险的DNA序列变化与胰腺细胞处理两种不同分子压力的能力有关。
胰腺细胞和人一样,只能承受一定的压力,然后就会开始崩溃。某些压力源,如炎症和高血糖,会使这些细胞不堪重负,从而导致2型糖尿病的发展。
杰克逊实验室(JAX)的研究人员现在发现,已知会增加一个人患糖尿病风险的DNA序列变化与胰腺细胞处理两种不同分子压力的能力有关。在有这些DNA变化的人身上,胰腺中产生胰岛素的细胞在暴露于压力和炎症时可能更容易衰竭或死亡。
JAX副教授Michael L. Stitzel和JAX教授Dugyu Ucar共同撰写了这项新研究,该研究发表在10月8日的《细胞代谢》高级在线版上,他说:“最终,我们希望通过针对最易患这种疾病的人的基因和途径,开发出预防和治疗2型糖尿病的新方法。”“这些发现让我们对其中一些基因和途径有了新的认识。”
这项工作指出了几十个与细胞压力和糖尿病风险有关的基因,其中一个基因已经在研究中,可以作为治疗2型糖尿病并发症的药物靶点。

图1 多组分人胰岛内质网和细胞因子应激反应图谱提供了2型糖尿病的遗传见解
压力下的细胞
当活细胞面临挑战,包括损伤、炎症或营养变化时,它们会激活保护性反应,试图应对和逆转压力。但随着时间的推移,持续的压力会压倒细胞,导致它们减缓或死亡。
在胰岛β细胞中,两种类型的细胞压力与2型糖尿病的发展有关。
内质网(ER)应激发生时,细胞变得不堪重负的高需求产生蛋白质,如胰岛素,以帮助调节血糖水平。
当免疫系统发出过多的炎症信号时,细胞因子压力就会发生——就像肥胖和代谢疾病一样。
在这两种情况下,压力最终会导致胰岛细胞停止产生胰岛素或死亡。
Stitzel和他的同事们想知道胰岛细胞使用了哪些基因和蛋白质来对内质网应激和细胞因子应激做出反应。
Stitzel说:“研究人员已经完成了多项研究,以了解哪些分子途径在调节快乐、健康的胰岛细胞的胰岛素分泌中起重要作用。”“但我们的假设是,胰岛细胞并不总是快乐的。那么,当细胞处于压力下时,哪些途径是重要的?我们每个人体内与糖尿病相关的DNA序列变化是如何影响它们的?”
应激反应的基因
Stitzel的研究小组将健康的人类胰岛细胞暴露于已知会引起内质网应激或细胞因子应激的化合物中。然后,他们追踪细胞中RNA分子水平的变化,以及细胞内不同DNA片段排列的紧密程度或松散程度——这是细胞在任何给定时间使用哪些基因和调控元件的代理。
为了分析结果,该团队与JAX的教授兼计算生物学家Ucar合作。科学家们共同发现,超过5000个基因,或健康胰岛细胞表达的所有基因的近三分之一,在内质网压力或细胞因子压力下改变了它们的表达。其中许多参与了蛋白质的产生,这对胰岛细胞产生胰岛素至关重要。大多数基因只参与一种或另一种应激反应,提出了两种不同的应激途径在糖尿病中起作用的观点。
此外,大约八分之一的用于胰岛细胞的DNA调节区域被压力改变。重要的是,这些调控区域中有86个先前被发现含有2型糖尿病高危人群的遗传变异。
Stitzel说:“这表明,具有这些基因变异的人的胰岛细胞对压力的反应可能比其他人更差。”“你的环境——比如糖尿病和肥胖——触发了2型糖尿病,但你的基因是扳机的扳机。”
Stitzel希望新的调控区域和基因列表最终能够通过潜在地使胰岛细胞更能适应压力而产生预防或治疗糖尿病的新药。

图2 人胰岛ER应激和细胞因子反应基因的综合比较图谱
一个可用药的目标
研究人员找到了一个被内质网应激改变的基因。该基因被称为MAP3K5,在胰岛素编码基因中含有引起糖尿病的突变的小鼠中,被证明可以改变胰岛β细胞的死亡。
在这篇新论文中,Stitzel和他的同事们表明,更高水平的MAP3K5导致更多的胰岛β细胞在内质网应激下死亡。另一方面,消除或阻断MAP3K5使胰岛细胞对内质网应激更有弹性,更不容易死亡。
针对MAP3K5的药物Selonsertib的早期研究表明,它可以降低糖尿病严重并发症的风险。新的研究结果指出了这种药物的另一个可能的作用——在糖尿病高危人群中预防糖尿病,帮助他们的胰岛细胞在细胞压力下保持功能和活力。
Stitzel说:“这种治疗方法已经在临床试验中,这确实令人兴奋,但要了解这种药物是否能够用于初级预防,还需要做更多的工作。”
参考资料
[1] Multi-omic human pancreatic islet endoplasmic reticulum and cytokine stress response mapping provides type 2 diabetes genetic insights



