摘要:一项研究揭示了膀胱癌的起源和发展过程
威尔康奈尔医学院和纽约基因组中心的研究人员领导的一项研究揭示了膀胱癌的起源和发展过程,这是前所未有的。研究人员发现,使正常细胞和癌细胞的DNA发生突变的抗病毒酶是早期膀胱癌发展的关键促进因素,而标准化疗也是突变的一个有力来源。研究人员还发现,肿瘤细胞中异常环状DNA结构中过度活跃的基因会导致膀胱癌对治疗产生耐药性。这些发现是对膀胱癌生物学的新见解,并为这种难以治疗的癌症提供了新的治疗策略。
这项研究发表在《自然》杂志上,重点研究了膀胱癌的主要形式——尿路上皮癌,它起源于膀胱、尿道和肾脏排尿管的细胞。研究人员检查了来自同一组处于不同疾病阶段的患者的恶性和恶性前尿路上皮细胞。他们使用全基因组测序和先进的计算方法来绘制常见的DNA突变、复杂的结构变异及其时间。

图1 突变与ecDNA形成尿路上皮癌症演变的相互作用
“我们的发现定义了驱动膀胱癌进化的新的基本机制——我们现在可以考虑靶向治疗的机制,”共同资深作者Bishoy Faltas博士说,他是盖勒特家族的约翰伦纳德医学博士血液学和医学肿瘤学研究学者,也是威尔康奈尔医学院的医学和细胞与发育生物学副教授,也是纽约长老会/威尔康奈尔医学中心的肿瘤学家。
纽约基因组中心(New York Genome Center)计算生物学主任Nicolas Robine博士,以及英国精密医学研究所Olivier Elemento博士,也共同领导了这项研究。共同第一作者是Duy Nguyen和纽约基因组中心的生物信息学科学家William Hooper,以及Weisi Liu博士。
主要治疗靶点成为焦点
在美国,膀胱癌的发病率约为每年8万例。如果发现得早,可以通过手术治愈,但大约30%的病例在晚期才被诊断出来,而晚期的治疗难度要大得多。
在这项新研究中,研究人员发现了强有力的证据,证明APOBEC3酶会导致早期突变,而这种突变可能有助于引发这种癌症的发展。这些酶的进化是通过编辑逆转录病毒的病毒DNA来阻止感染逆转录病毒,尽管众所周知,它们有时会使细胞自身的DNA发生突变。
“apobec3诱导的突变在癌症发生中的确切作用还不清楚,但我们发现这些突变出现在尿路上皮癌的早期,甚至发生在恶性前尿路上皮组织中。”在Faltas实验室里,Faltas博士专注于研究这些致突变酶在推动癌症进化中的作用。
研究人员发现,顺铂和其他以铂为基础的化疗引起进一步的显著突变爆发,其中一些可能使尿路上皮癌细胞在治疗后更好地存活和扩散。
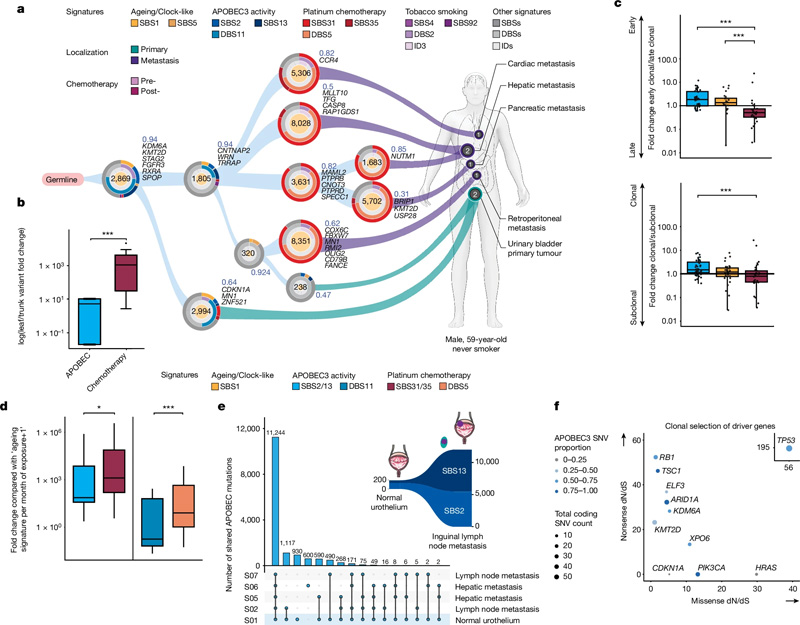
图2 UC进化中的诱变过程
第三个主要发现是,尿路上皮肿瘤通常包含复杂的DNA重排,从而产生环状DNA片段。这些“染色体外dna”(ecdna)与细胞核中的染色体分开存在,有时可以携带数百个驱动癌症的生长基因拷贝。研究人员发现,这些ecDNA事件持续存在并变得更加复杂,在治疗后合并了新的DNA片段,这表明它们会导致对治疗的抵抗。
这促使研究小组在实验室中对这些基因中的一种称为CCND1的ecDNA版本进行实验模拟,CCND1是细胞周期的主要调节因子。这些实验的结果证实,CCND1在这种染色体外配置驱动治疗耐药性。
总之,这些发现更清晰地描绘了引发和驱动尿路上皮癌的因素。
“传统上,在分析肿瘤基因组时,我们使用的方法只分析其DNA的一小部分,但我们已经意识到,如果我们对所有的DNA进行测序,并使用智能方法来评估这些数据,还有更多的东西需要发现,”Elemento博士说。“我认为这次合作证明了这一战略的正确性。”
英格兰研究所和纽约基因组中心的研究人员正在计划未来更大规模的合作研究,以更深入地挖掘尿路上皮癌生物学,例如,不仅在大量肿瘤样本中,而且在单个肿瘤细胞中,对DNA进行全基因组测序,并读出基因活性。
“在单细胞水平上将这两组信息结合起来将是非常重要和有趣的”。
研究人员还计划研究这项工作的潜在临床应用。研究人员希望FDA批准的一种靶向ERBB2基因产物的新药物——HER2受体蛋白,也在乳腺肿瘤细胞中发现——对具有强烈ERBB2 ecdna迹象的尿路上皮癌患者尤其有效。他们也在努力寻找阻断ecDNA形成和维持的方法。
参考资料
[1] The interplay of mutagenesis and ecDNA shapes urothelial cancer evolution
摘要:一项研究揭示了膀胱癌的起源和发展过程
威尔康奈尔医学院和纽约基因组中心的研究人员领导的一项研究揭示了膀胱癌的起源和发展过程,这是前所未有的。研究人员发现,使正常细胞和癌细胞的DNA发生突变的抗病毒酶是早期膀胱癌发展的关键促进因素,而标准化疗也是突变的一个有力来源。研究人员还发现,肿瘤细胞中异常环状DNA结构中过度活跃的基因会导致膀胱癌对治疗产生耐药性。这些发现是对膀胱癌生物学的新见解,并为这种难以治疗的癌症提供了新的治疗策略。
这项研究发表在《自然》杂志上,重点研究了膀胱癌的主要形式——尿路上皮癌,它起源于膀胱、尿道和肾脏排尿管的细胞。研究人员检查了来自同一组处于不同疾病阶段的患者的恶性和恶性前尿路上皮细胞。他们使用全基因组测序和先进的计算方法来绘制常见的DNA突变、复杂的结构变异及其时间。

图1 突变与ecDNA形成尿路上皮癌症演变的相互作用
“我们的发现定义了驱动膀胱癌进化的新的基本机制——我们现在可以考虑靶向治疗的机制,”共同资深作者Bishoy Faltas博士说,他是盖勒特家族的约翰伦纳德医学博士血液学和医学肿瘤学研究学者,也是威尔康奈尔医学院的医学和细胞与发育生物学副教授,也是纽约长老会/威尔康奈尔医学中心的肿瘤学家。
纽约基因组中心(New York Genome Center)计算生物学主任Nicolas Robine博士,以及英国精密医学研究所Olivier Elemento博士,也共同领导了这项研究。共同第一作者是Duy Nguyen和纽约基因组中心的生物信息学科学家William Hooper,以及Weisi Liu博士。
主要治疗靶点成为焦点
在美国,膀胱癌的发病率约为每年8万例。如果发现得早,可以通过手术治愈,但大约30%的病例在晚期才被诊断出来,而晚期的治疗难度要大得多。
在这项新研究中,研究人员发现了强有力的证据,证明APOBEC3酶会导致早期突变,而这种突变可能有助于引发这种癌症的发展。这些酶的进化是通过编辑逆转录病毒的病毒DNA来阻止感染逆转录病毒,尽管众所周知,它们有时会使细胞自身的DNA发生突变。
“apobec3诱导的突变在癌症发生中的确切作用还不清楚,但我们发现这些突变出现在尿路上皮癌的早期,甚至发生在恶性前尿路上皮组织中。”在Faltas实验室里,Faltas博士专注于研究这些致突变酶在推动癌症进化中的作用。
研究人员发现,顺铂和其他以铂为基础的化疗引起进一步的显著突变爆发,其中一些可能使尿路上皮癌细胞在治疗后更好地存活和扩散。

图2 UC进化中的诱变过程
第三个主要发现是,尿路上皮肿瘤通常包含复杂的DNA重排,从而产生环状DNA片段。这些“染色体外dna”(ecdna)与细胞核中的染色体分开存在,有时可以携带数百个驱动癌症的生长基因拷贝。研究人员发现,这些ecDNA事件持续存在并变得更加复杂,在治疗后合并了新的DNA片段,这表明它们会导致对治疗的抵抗。
这促使研究小组在实验室中对这些基因中的一种称为CCND1的ecDNA版本进行实验模拟,CCND1是细胞周期的主要调节因子。这些实验的结果证实,CCND1在这种染色体外配置驱动治疗耐药性。
总之,这些发现更清晰地描绘了引发和驱动尿路上皮癌的因素。
“传统上,在分析肿瘤基因组时,我们使用的方法只分析其DNA的一小部分,但我们已经意识到,如果我们对所有的DNA进行测序,并使用智能方法来评估这些数据,还有更多的东西需要发现,”Elemento博士说。“我认为这次合作证明了这一战略的正确性。”
英格兰研究所和纽约基因组中心的研究人员正在计划未来更大规模的合作研究,以更深入地挖掘尿路上皮癌生物学,例如,不仅在大量肿瘤样本中,而且在单个肿瘤细胞中,对DNA进行全基因组测序,并读出基因活性。
“在单细胞水平上将这两组信息结合起来将是非常重要和有趣的”。
研究人员还计划研究这项工作的潜在临床应用。研究人员希望FDA批准的一种靶向ERBB2基因产物的新药物——HER2受体蛋白,也在乳腺肿瘤细胞中发现——对具有强烈ERBB2 ecdna迹象的尿路上皮癌患者尤其有效。他们也在努力寻找阻断ecDNA形成和维持的方法。
参考资料
[1] The interplay of mutagenesis and ecDNA shapes urothelial cancer evolution



