摘要:新研究发现通常会为免疫系统踩刹车以防止其攻击人体健康细胞的免疫细胞亚群也会无意中抑制癌症免疫疗法。
通过调动免疫系统来对抗肿瘤细胞,免疫疗法提高了生存率,为数百万癌症患者带来了希望。然而,只有大约五分之一的人对这些治疗反应良好。
为了了解和解决免疫疗法的局限性,圣路易斯华盛顿大学医学院的研究人员发现,免疫系统在对抗癌症的过程中可能是自己最大的敌人。在一项针对小鼠的新研究中,免疫细胞的一个子集——1型调节性T细胞(Tr1细胞),正常地阻止免疫系统过度反应,但在这样做的同时,无意中抑制了免疫疗法的抗癌能力。

图1 新抗原特异性细胞毒性Tr1 CD4 T细胞抑制癌症免疫疗法
资深作者Robert D. Schreiber博士说:“Tr1细胞被发现是免疫疗法对癌症有效性的一个迄今为止未被认识到的障碍。通过移除或绕过小鼠体内的这一屏障,我们成功地重新激活了免疫系统的抗癌细胞,并为更多癌症患者提供了扩大免疫疗法益处的机会。”
这项研究发表在《自然》杂志上。
癌症疫苗是个体化癌症免疫治疗的一种新途径。这类疫苗针对患者肿瘤的特异性突变蛋白,诱导杀伤T细胞攻击肿瘤细胞,同时不伤害健康细胞。
Schreiber的研究小组先前表明,更有效的疫苗还可以激活辅助T细胞,这是另一种免疫细胞类型,可以招募和扩大额外的杀伤T细胞来摧毁肿瘤。但是当他们试图增加辅助T细胞目标的数量来增强疫苗时,他们发现产生了一种不同类型的T细胞,这种T细胞抑制而不是促进了肿瘤的排斥反应。
“我们测试了这样一个假设,即通过增加辅助性T细胞的激活,我们可以诱导小鼠肉瘤肿瘤的增强消除,”第一作者Hussein Sultan博士说。因此,他给几组携带肿瘤的小鼠注射了疫苗,这些疫苗可以同等程度地激活杀伤T细胞,同时触发不同程度的辅助T细胞激活。
在这项最新的研究中,让研究人员感到惊讶的是,旨在过度激活辅助性T细胞的疫苗产生了相反的效果,抑制了肿瘤的排斥反应。
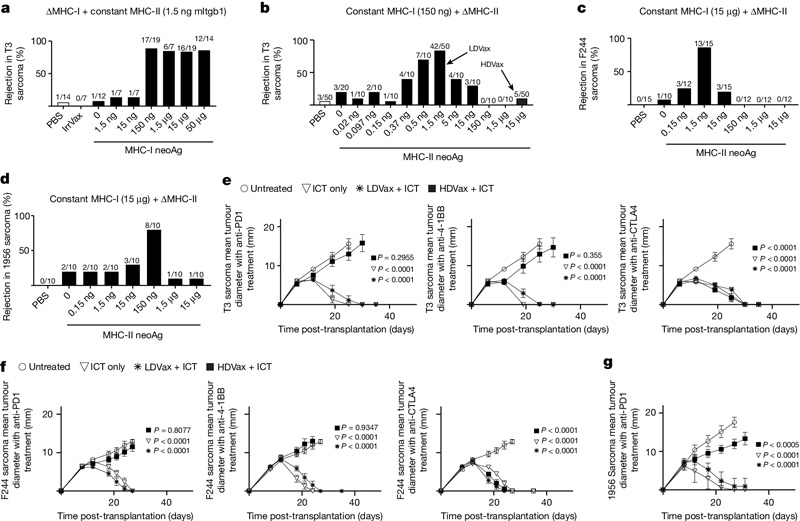
图2 高剂量的MHC-II neoAg会抑制SLP疫苗和某些ICT的抗肿瘤疗效
“我们认为更多的辅助T细胞激活将优化小鼠肉瘤肿瘤的消除,相反,我们发现含有高剂量辅助性T细胞靶点的疫苗诱导了完全阻断肿瘤消除的抑制性Tr1细胞。我们知道Tr1细胞通常控制过度活跃的免疫系统,但这是它们第一次被证明可以抑制免疫系统对抗癌症。”
通常情况下,Tr1细胞会对免疫系统起到抑制作用,防止它攻击身体的健康细胞。但它们在癌症中的作用尚未得到认真探讨。通过查阅先前发表的数据,研究人员发现,与对免疫治疗反应良好的患者的肿瘤相比,对免疫治疗反应较差的患者的肿瘤有更多的Tr1细胞。随着肿瘤变大,小鼠体内Tr1细胞的数量也会增加,使小鼠对免疫治疗不敏感。
为了绕过抑制细胞,研究人员用一种增强杀伤T细胞战斗力的药物治疗接种了疫苗的小鼠。这种药物是由生物技术初创公司Asher biotheraptics开发的,它在一种叫做白细胞介素2 (IL-2)的免疫增强蛋白中进行了修饰,这种蛋白可以特异性地加速杀伤性T细胞,降低未经修饰的IL-2治疗的毒性。该药的额外作用克服了Tr1细胞的抑制作用,使免疫疗法更加有效。
Schreiber说:“我们致力于个性化免疫疗法并扩大其有效性。几十年的基础肿瘤免疫学研究扩大了我们对如何触发免疫系统以实现最强大的抗肿瘤反应的理解。这项新研究增加了我们对如何改进免疫疗法以使更多人受益的理解。”
作为Asher Biotherapeutics的联合创始人,Schreiber间接参与了该公司的临床试验,测试人类版本的药物作为癌症患者的单一疗法。Asher Biotherapeutics提供了小鼠版本的改良IL-2药物。如果成功,这种药物将有可能与癌症治疗疫苗联合进行测试。
参考资料
[1] Neoantigen-specific cytotoxic Tr1 CD4 T cells suppress cancer immunotherapy
摘要:新研究发现通常会为免疫系统踩刹车以防止其攻击人体健康细胞的免疫细胞亚群也会无意中抑制癌症免疫疗法。
通过调动免疫系统来对抗肿瘤细胞,免疫疗法提高了生存率,为数百万癌症患者带来了希望。然而,只有大约五分之一的人对这些治疗反应良好。
为了了解和解决免疫疗法的局限性,圣路易斯华盛顿大学医学院的研究人员发现,免疫系统在对抗癌症的过程中可能是自己最大的敌人。在一项针对小鼠的新研究中,免疫细胞的一个子集——1型调节性T细胞(Tr1细胞),正常地阻止免疫系统过度反应,但在这样做的同时,无意中抑制了免疫疗法的抗癌能力。

图1 新抗原特异性细胞毒性Tr1 CD4 T细胞抑制癌症免疫疗法
资深作者Robert D. Schreiber博士说:“Tr1细胞被发现是免疫疗法对癌症有效性的一个迄今为止未被认识到的障碍。通过移除或绕过小鼠体内的这一屏障,我们成功地重新激活了免疫系统的抗癌细胞,并为更多癌症患者提供了扩大免疫疗法益处的机会。”
这项研究发表在《自然》杂志上。
癌症疫苗是个体化癌症免疫治疗的一种新途径。这类疫苗针对患者肿瘤的特异性突变蛋白,诱导杀伤T细胞攻击肿瘤细胞,同时不伤害健康细胞。
Schreiber的研究小组先前表明,更有效的疫苗还可以激活辅助T细胞,这是另一种免疫细胞类型,可以招募和扩大额外的杀伤T细胞来摧毁肿瘤。但是当他们试图增加辅助T细胞目标的数量来增强疫苗时,他们发现产生了一种不同类型的T细胞,这种T细胞抑制而不是促进了肿瘤的排斥反应。
“我们测试了这样一个假设,即通过增加辅助性T细胞的激活,我们可以诱导小鼠肉瘤肿瘤的增强消除,”第一作者Hussein Sultan博士说。因此,他给几组携带肿瘤的小鼠注射了疫苗,这些疫苗可以同等程度地激活杀伤T细胞,同时触发不同程度的辅助T细胞激活。
在这项最新的研究中,让研究人员感到惊讶的是,旨在过度激活辅助性T细胞的疫苗产生了相反的效果,抑制了肿瘤的排斥反应。

图2 高剂量的MHC-II neoAg会抑制SLP疫苗和某些ICT的抗肿瘤疗效
“我们认为更多的辅助T细胞激活将优化小鼠肉瘤肿瘤的消除,相反,我们发现含有高剂量辅助性T细胞靶点的疫苗诱导了完全阻断肿瘤消除的抑制性Tr1细胞。我们知道Tr1细胞通常控制过度活跃的免疫系统,但这是它们第一次被证明可以抑制免疫系统对抗癌症。”
通常情况下,Tr1细胞会对免疫系统起到抑制作用,防止它攻击身体的健康细胞。但它们在癌症中的作用尚未得到认真探讨。通过查阅先前发表的数据,研究人员发现,与对免疫治疗反应良好的患者的肿瘤相比,对免疫治疗反应较差的患者的肿瘤有更多的Tr1细胞。随着肿瘤变大,小鼠体内Tr1细胞的数量也会增加,使小鼠对免疫治疗不敏感。
为了绕过抑制细胞,研究人员用一种增强杀伤T细胞战斗力的药物治疗接种了疫苗的小鼠。这种药物是由生物技术初创公司Asher biotheraptics开发的,它在一种叫做白细胞介素2 (IL-2)的免疫增强蛋白中进行了修饰,这种蛋白可以特异性地加速杀伤性T细胞,降低未经修饰的IL-2治疗的毒性。该药的额外作用克服了Tr1细胞的抑制作用,使免疫疗法更加有效。
Schreiber说:“我们致力于个性化免疫疗法并扩大其有效性。几十年的基础肿瘤免疫学研究扩大了我们对如何触发免疫系统以实现最强大的抗肿瘤反应的理解。这项新研究增加了我们对如何改进免疫疗法以使更多人受益的理解。”
作为Asher Biotherapeutics的联合创始人,Schreiber间接参与了该公司的临床试验,测试人类版本的药物作为癌症患者的单一疗法。Asher Biotherapeutics提供了小鼠版本的改良IL-2药物。如果成功,这种药物将有可能与癌症治疗疫苗联合进行测试。
参考资料
[1] Neoantigen-specific cytotoxic Tr1 CD4 T cells suppress cancer immunotherapy



